题目内容
17.盐酸是一种用途广泛的物质,在实验室中用盐酸与其他物质反应可以制得多种气体,其中一种气体的化学式是CO2,写出制取该气体的化学反应方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;盐酸在工业上有多种用途,其中一种用途是金属表面除锈.分析 根据稀盐酸能和锌反应生成氯化锌和氢气,稀盐酸能和碳酸钙反应生成氯化钙、水和二氧化碳;稀盐酸能和氧化铁反应,常用于除锈进行分析.
解答 解:利用稀盐酸和锌反应可以制取氢气,利用稀盐酸和碳酸钙反应可以制取二氧化碳,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑,CaCO3+2HCl═CaCl2+H2O+CO2↑;盐酸会与金属氧化物反应,所以稀盐酸常用于除锈.
故答案为:CO2,CaCO3+2HCl═CaCl2+H2O+CO2↑,金属表面除锈等.
点评 酸具有一些相似的化学性质,例如能使石蕊试液变红色,能和某些金属单质、某些金属氧化物、某些盐、碱反应生成相应的物质.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
5.化学与生活息息相关,生活中处处涉及化学
(1)下列生活“小贴士”中的化学运用正确的是②④.
①春天播种;及时施碳铵(NH4HCO3)与草木灰(K2CO3)混合肥以增肥效
②夏天炎热;鱼池及时充氧以防缺氧
③秋天水果成熟;及时增施农药以保收成
④寒冬积雪;公路及时撒盐以保安全
(2)透视时通常服用一种乳白色的液体“钡餐”,其主要成分是BaSO4,该液体属于悬浊液(填“溶液”、“乳浊液”、“悬浊液”); 已知含Ba2+的溶液会使人中毒,若误服BaCO3会中毒,这是由于BaCO3+2HCl=BaCl2+H2O+CO2↑(填化学方程式),若误服,应立即服泻盐MgSO4,其理由是(填化学方程式)BaCl2+MgSO4=BaSO4↓+2MgCl.
(3)人体中的胃液主要成分是盐酸,过多会导致胃痛,特别是胃溃疡患者尤为严重,其应服用含【填NaOH、NaHCO3、Al(OH)3】的药物.其治疗原理是Al(OH)3+3HCl=AlCl3+3H2O(填化学方程式).
(4)用熟石灰中和一定量含盐酸的废水,溶液的pH与加入的熟石灰质量的关系如图1所示,熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O;若改用mg氢氧化钠与相同量的废水反应,所得溶液的pH<7(填“>”“<”或“=”).
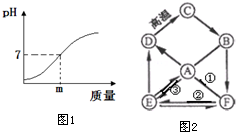
(5)A、B、C、D、E、F均为初中化学常见的物质,已知D在生活中常用作补钙剂和建筑材料,F为NaOH,它们之间存在的转化关系如图2,其中“→”表示由某种物质可转化为另一种物质,“-”表示两物质之间可以相互反应(部分反应物、生成物及反应条件已略去)其中.请按要求回答下列问题.
①用化学式表示:ENa2CO3;
②写出C→B的化学方程式是CaO+H2O=Ca(OH)2;
③题中没有涉及的化学基本反应类型是置换反应.
(6)实验室有甲、乙、丙三瓶溶液,分别含有以下六种物质中的两种:KOH、HNO3、AgNO3、KCl、K2SO4、Ba(NO3)2.经初步分析,情况如下:
为了进一步确定各溶液的组成,进行如下实验:(①已知溶液中不可能同时存在Ag+和OH-,②AgNO3显酸性,③两次混合均完全反应).根据以上信息回答:
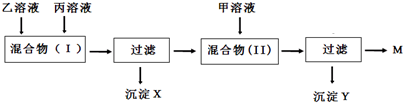
①甲溶液中肯定含有的物质是KOH(填化学式,下同),含有的另一种物质是K2SO4(或KCl),据此,沉淀X是AgCl(或BaSO4);
②根据(Ⅰ)的判断,混合(Ⅱ)中产生沉淀的化学方程式为:K2SO4+Ba(NO3)2═BaSO4↓+2KNO3;HNO3+KOH═H2O+KNO3或KCl+AgNO3═AgCl↓+KNO3;HNO3+KOH═H2O+KNO3;
③溶液M中溶质的化学式KNO3,它是一种复合肥,含有农作物所需的营养元素是K、N(填元素符号).
(1)下列生活“小贴士”中的化学运用正确的是②④.
①春天播种;及时施碳铵(NH4HCO3)与草木灰(K2CO3)混合肥以增肥效
②夏天炎热;鱼池及时充氧以防缺氧
③秋天水果成熟;及时增施农药以保收成
④寒冬积雪;公路及时撒盐以保安全
(2)透视时通常服用一种乳白色的液体“钡餐”,其主要成分是BaSO4,该液体属于悬浊液(填“溶液”、“乳浊液”、“悬浊液”); 已知含Ba2+的溶液会使人中毒,若误服BaCO3会中毒,这是由于BaCO3+2HCl=BaCl2+H2O+CO2↑(填化学方程式),若误服,应立即服泻盐MgSO4,其理由是(填化学方程式)BaCl2+MgSO4=BaSO4↓+2MgCl.
(3)人体中的胃液主要成分是盐酸,过多会导致胃痛,特别是胃溃疡患者尤为严重,其应服用含【填NaOH、NaHCO3、Al(OH)3】的药物.其治疗原理是Al(OH)3+3HCl=AlCl3+3H2O(填化学方程式).
(4)用熟石灰中和一定量含盐酸的废水,溶液的pH与加入的熟石灰质量的关系如图1所示,熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O;若改用mg氢氧化钠与相同量的废水反应,所得溶液的pH<7(填“>”“<”或“=”).

(5)A、B、C、D、E、F均为初中化学常见的物质,已知D在生活中常用作补钙剂和建筑材料,F为NaOH,它们之间存在的转化关系如图2,其中“→”表示由某种物质可转化为另一种物质,“-”表示两物质之间可以相互反应(部分反应物、生成物及反应条件已略去)其中.请按要求回答下列问题.
①用化学式表示:ENa2CO3;
②写出C→B的化学方程式是CaO+H2O=Ca(OH)2;
③题中没有涉及的化学基本反应类型是置换反应.
(6)实验室有甲、乙、丙三瓶溶液,分别含有以下六种物质中的两种:KOH、HNO3、AgNO3、KCl、K2SO4、Ba(NO3)2.经初步分析,情况如下:
| 溶液 | 外观 | pH | 溶液成分 | |
| 甲 | 无色、透明 | >7 | ? | ? |
| 乙 | 无色、透明 | =7 | Ba(NO3)2 | ? |
| 丙 | 无色、透明 | <7 | ? | ? |

①甲溶液中肯定含有的物质是KOH(填化学式,下同),含有的另一种物质是K2SO4(或KCl),据此,沉淀X是AgCl(或BaSO4);
②根据(Ⅰ)的判断,混合(Ⅱ)中产生沉淀的化学方程式为:K2SO4+Ba(NO3)2═BaSO4↓+2KNO3;HNO3+KOH═H2O+KNO3或KCl+AgNO3═AgCl↓+KNO3;HNO3+KOH═H2O+KNO3;
③溶液M中溶质的化学式KNO3,它是一种复合肥,含有农作物所需的营养元素是K、N(填元素符号).
2.在密闭容器中,7.2g碳与一定量氧气恰好完全反应,生成气体的质量可能是( )
| A. | 8.4g | B. | 17.8g | C. | 26.4g | D. | 44g |
15.以下叙述不正确的是( )
| A. | 钛和钛合金是制造飞机和轮船的理想材料 | |
| B. | 钙是人体中含量最多的金属元素 | |
| C. | 黄铜是铜、锌合金,它的硬度大于铜 | |
| D. | 焊锡的熔点比锡和铅都高 |
16.下列说法正确的是( )
| A. | 能使石蕊溶液变蓝的溶液都是碱溶液 | |
| B. | 一种元素只能组成一种物质 | |
| C. | 同一种元素的原子和离子的化学性质相同 | |
| D. | 水果和蔬菜都富含维生素 |
 ;
;