题目内容
在X+2O2
CO2+2H2O的反应中,根据质量守恒定律可判断出X的化学式为( )
| ||
| A、CO |
| B、CH4 |
| C、CH3OH |
| D、C2H4 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律可知,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
根据化学方程式和质量守恒定律就可计算出生成物各元素的原子个数与反应物各元素的原子个数之差,就是X的化学式中含有的元素的原子个数.
然后对照选项进行选择即可.
根据化学方程式和质量守恒定律就可计算出生成物各元素的原子个数与反应物各元素的原子个数之差,就是X的化学式中含有的元素的原子个数.
然后对照选项进行选择即可.
解答:解:
根据化学方程式和质量守恒定律可知,X的化学式中含有的C元素的原子个数为1,H元素的原子个数为:2×2=4.故X的化学式为CH4
故选:B.
根据化学方程式和质量守恒定律可知,X的化学式中含有的C元素的原子个数为1,H元素的原子个数为:2×2=4.故X的化学式为CH4
故选:B.
点评:本题主要考查学生根据化学方程式和质量守恒定律解答问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如图的实验装置或操作正确的是( )
A、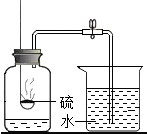 空气中氧气含量测定 |
B、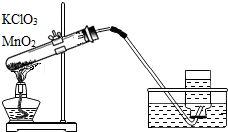 制取O2 |
C、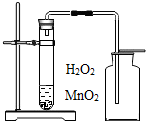 制取O2 |
D、 铁丝燃烧 |
现在很多人都愿意使用铁锅做饭炒菜,其原因是 ( )
①铁具有良好的导热性 ②铁资源丰富,价格低廉 ③食物中增加微量铁元素 ④铁在干燥空气中不易生锈.
①铁具有良好的导热性 ②铁资源丰富,价格低廉 ③食物中增加微量铁元素 ④铁在干燥空气中不易生锈.
| A、只有① | B、只有② |
| C、①②③ | D、①②③④ |
下表是人体几种重要体液的正常pH范围,其中酸性最强的是( )
| 体液 | 唾液 | 胃液 | 血液 | 胆汁 |
| 正常pH范围 | 6.6~7.1 | 0.8~1.5 | 7.35-7.45 | 6.8~7.4 |
| A、唾液 | B、胃液 | C、血液 | D、胆汁 |
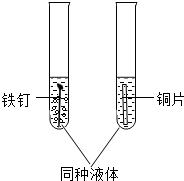 为了验证铁、铜两种金属的活动性差异,如图所示取2支试管分别进行有关实验,若要观察到现象的显著差异,所用液体合理的是( )
为了验证铁、铜两种金属的活动性差异,如图所示取2支试管分别进行有关实验,若要观察到现象的显著差异,所用液体合理的是( )| A、蒸馏水 | B、稀盐酸 |
| C、酒精水溶液 | D、蔗糖溶液 |
微型录像带的磁粉主要成分是化合物CoFe2O4,(铁元素显一个价态)则其中钴元素(Co)的化合价为( )
| A、+2 | B、+3 | C、+5 | D、+6 |

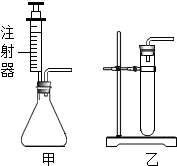
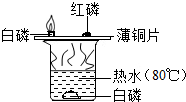 小明用如图所示装置探究可燃物燃烧的条件.他发现热水中的白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷及水中的白磷都不能燃烧.请回答:
小明用如图所示装置探究可燃物燃烧的条件.他发现热水中的白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷及水中的白磷都不能燃烧.请回答: