题目内容
2. 某科学兴趣小组查阅资料得知镁可在氧气中燃烧生成氧化镁,可在氮气中燃烧生成氮化镁,于是设计了如下方案进行验证.
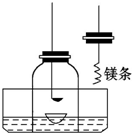
某科学兴趣小组查阅资料得知镁可在氧气中燃烧生成氧化镁,可在氮气中燃烧生成氮化镁,于是设计了如下方案进行验证.步骤1:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如图所示的装置.另准备一只有一根铜丝穿过的橡皮塞,铜丝末端固定一根镁条.
步骤2:引燃燃烧匙中足量的红磷,塞好橡皮塞.待充分冷却,观察到广口瓶内水面上升的体积约占原瓶内水面上方空间的$\frac{1}{5}$左右.
步骤3:往水槽中加水使广口瓶内外水面相平.点燃镁条,更换橡皮塞,镁条在广口瓶内继续燃烧,发出红光,放出热量.待冷却后广口瓶内水位继续上升.
(1)步骤2的目的是除去广口瓶内空气中的氧气.
(2)在步骤3“待冷却后广口瓶内水位继续上升”是由于瓶内气压小于(选填“大于”“小于”或“等于”)外界气压.
(3)根据上述实验和你所学的知识,请写出镁在空气中燃烧时的文字表达式:镁+氧气$\stackrel{点燃}{→}$氧化镁;镁+氮气$\stackrel{点燃}{→}$氮化镁.
(4)拓展应用
①通过该实验可知,不能(填“能”或“不能”)用镁条代替红磷测定空气中氧气的体积分数,若使用镁条,则测得结果偏大(填“偏大”或“偏小”);
②由此实验可知,选取代替红磷测定空气中氧气的体积分数的可燃物应具有的条件为只能与空气中的氧气反应.
分析 (1)根据实验目的可以知道是验证氮气可以和镁反应的,所以要排除氧气干扰实验现象,据此可以完成该题的解答;
(2)广口瓶中的水位上升,说明瓶内外产生了压强差,可以据此答题;
(3)根据实验可得出镁可以和氮气反应,故可以写出文字表达式;
(4)镁燃烧时,既能够消耗氧气,又能够消耗氮气,不能用镁条代替红磷测定空气中氧气的体积分数;
因为是测定空气中氧气的体积分数,所以选择的药品应该只能够和氧气发生反应
解答 解:(1)氧气可以和镁反应,所以要能够准确的判断出镁确实与氮气发生了反应,必须先排除氧气的干扰;
(2)广口瓶中的水位上升,说明瓶内的压强小于外界大气压,由于氧气已被消耗掉,所以同时也说明了镁和氮气发生了反应;
(3)根据实验现象可以判断镁在空气中可以和氧气及氮气发生反应,生成氧化镁和氮化镁.文字表达式为镁+氧气$\stackrel{点燃}{→}$氧化镁 镁+氮气$\stackrel{点燃}{→}$氮化镁
(4)①通过该实验可知,不能用镁条代替红磷测定空气中氧气的体积分数;
若使用镁条,镁条燃烧同时消耗氧气和氮气,会使测定的结果偏大.
②由此实验可知,选取代替红磷测定空气中氧气的体积分数的可燃物应具有的性质为只能与空气中的氧气反应.
故答案为:(1)除去广口瓶内空气中的氧气; (2)小于;
(3)镁+氧气$\stackrel{点燃}{→}$氧化镁; 镁+氮气$\stackrel{点燃}{→}$氮化镁;
(4)①不能 偏大 ②只能与空气中的氧气反应.
点评 根据实验步骤来判断实验目的是我们必需具备的能力,也是解决实验探究题的方法之一,在平时的学习过程中要注意加强这方面的培养与训练.

练习册系列答案
相关题目
13.小明从化学方程式2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑中总结的信息有:①参加反应的物质是水和氧气;②反应能在常温下进行; ③反应前后原子的总数不变 ④反应前后物质的种类不变;⑤二氧化锰是该反应的催化剂,其质量和性质在化学反应前后不变;⑥每68份质量的过氧化氢完全反应后,能生成36份质量的水和32份质量的氧气.其中正确的是( )
| A. | ②③⑥ | B. | ①②④⑤⑥ | C. | ①③④⑥ | D. | ①②③④ |
10.我们吃到的味道鲜美的鱼,是这样烹饪出来的:将洗净的鱼煎过后,再加入少许食醋、料酒、生姜、葱、食盐等加热.共热时发生了许多化学反应.其中,食醋中乙酸(CH3COOH)与料酒中乙醇(C2H5OH)发生化学反应,生成了有特殊香味的乙酸乙酯(CH3COOC2H5),下列有关说法正确的是( )
| A. | 乙酸乙酯是一种混合物 | |
| B. | 乙醇中碳、氢、氧三种元素的质量比为2:6:1 | |
| C. | 乙酸乙酯是由碳、氢、氧三种原子构成的化合物 | |
| D. | 乙酸是由碳、氢、氧三种元素组成的 |
17.从物质组成的角度看,与臭氧、红磷、铁属于同一类别的是( )
| A. | 二氧化硫 | B. | 冰 | C. | 液氮 | D. | 空气 |
11.下列叙述中,属于物质化学性质的是( )
| A. | 铁在潮湿的空气中易生锈 | B. | 铜具有导电性 | ||
| C. | 水在4℃密度最大(1g/cm3) | D. | 食盐易溶于水 |
 如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,B能用于灭火,“-”表示相连两物质之间能相互反应.
如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,B能用于灭火,“-”表示相连两物质之间能相互反应.