题目内容
3.把A、B、C、D四种纯净物放在一密闭容器中,在一定条件下充分反应,反应前后各物质的质量如下表:| 物质 | A | B | C | D |
| 反应前质量/g | 2 | 25 | 2 | 1 |
| 反应后质量/g | 18 | 0 | 2 | 未知 |
(1)反应后D的质量是10g;
(2)C物质可能是催化剂(填写反应物、生成物或催化剂);
(3)容器中发生反应的反应类型是分解反应(填写基本反应类型).
分析 本题可分析先A、B、C三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定D是反应物还是生成物,进而可以确定反应类型.
解答 解:表中数据分析可知,反应前后,A的质量增加了18g-2g=16g,故A是生成物,参加反应的A的质量为16g;B的质量减少了25g-0g=25g,故B是反应物,参加反应的B的质量为25g;C的质量反应前后不变,C可能作该反应的催化剂,也可能没有参加反应;由质量守恒定律,D应是生成物,且生成的D的质量为25g-16g=9g,故待测D的质量为1+9g=10g.该反应的反应物为B,生成物是A和D,符合“一变多”的特征,属于分解反应.
(1)反应后D的质量是1+9g=10g;
(2)根据分析,C的质量反应前后不变,故C物质可能是催化剂;
(3)根据分析,该反应的反应物为B,生成物是A和D,符合“一变多”的特征,故容器中发生反应的反应类型是分解反应.
故答案为:
(1)10;(2)催化剂;(3)分解反应.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
相关题目
18.一种焰火火药中所含的硝酸铜在燃放时产生绿色火焰,发生如下反应:2Cu(NO3)2$\frac{\underline{\;点燃\;}}{\;}$2CuO+O2↑+4X↑.下列有关说法错误的是( )
| A. | 该反应的基本类型为分解反应 | |
| B. | 产物中CuO属于氧化物 | |
| C. | Cu(NO3)2中铜元素的化合价为+2 | |
| D. | 根据质量守恒定律推知X的化学式为NO |
15.类推是学习化学的一种重要方法,下列正确的是( )
| A. | 离子是带电的粒子,所以带电的粒子一定是离子 | |
| B. | 燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| C. | 点燃氢气、甲烷前需验纯,所以点燃任何可燃性气体前都需验纯 | |
| D. | 燃烧过程伴随发光、放热现象,所以有发光、放热现象的变化都是燃烧 |
12.下列说法正确的是( )
| A. | 水电解生成氢气和氧气,说明水中含有氢分子和氧分子 | |
| B. | 在水的电解反应中,氢原子和氧原子没有发生变化 | |
| C. | 水的蒸发和水的电解都有生成气体,它们都是化学变化 | |
| D. | 物质在变化中表现出来的性质,都是物质的化学性质 |
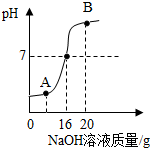 实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算:
实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算: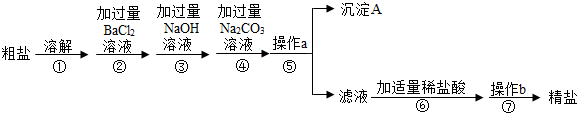
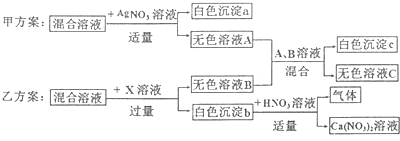
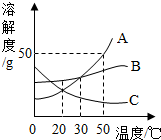 请根据图中A、B、C三种物质的溶解度曲线,回答下列问题.
请根据图中A、B、C三种物质的溶解度曲线,回答下列问题.