题目内容
15.打开酒精灯能闻到酒精的气味,其主要原因是( )| A. | 分子的质量很小 | B. | 分子不断地运动 | C. | 分子由原子构成 | D. | 分子之间有间隔 |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
解答 解:A、打开酒精灯能闻到酒精的气味,是因为酒精分子是在不断的运动的,向四周扩散,使人们闻到酒精的气味,而不是分子的质量很小,故选项错误.
B、打开酒精灯能闻到酒精的气味,是因为酒精分子是在不断的运动的,向四周扩散,使人们闻到酒精的气味,故选项正确.
C、打开酒精灯能闻到酒精的气味,是因为酒精分子是在不断的运动的,向四周扩散,使人们闻到酒精的气味,而不是分子由原子构成,故选项错误.
D、打开酒精灯能闻到酒精的气味,是因为酒精分子是在不断的运动的,向四周扩散,使人们闻到酒精的气味,而不是分子之间有间隔,故选项错误.
故选:B.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
相关题目
5.下列关于氧气的说法正确的是( )
| A. | 氧气能支持燃烧,可用作燃料 | |
| B. | 在空气稀薄的青藏高原,氧气的体积分数仍是21% | |
| C. | 氧气易溶于水,使水生动物得以生存 | |
| D. | 氧气能跟所有的物质发生氧化反应 |
3.3月29日是2014年度的“地球一小时”活动日,主题为“蓝天自造”,旨在呼吁每一位公民从自身开始,采取实际行动,应对当前中国最急迫、最受关注的环境问题-雾霾.下列做法不符合这一主题的是( )
| A. | 尽量少使用一次性塑料袋 | B. | 将落叶收集起来,一次性焚烧 | ||
| C. | 选择自行车和公交车作为出行工具 | D. | 用电子贺卡代替纸质贺卡 |
10.分离、除杂和检验是化学实验的重要环节.下面实验设计能够达到目的是( )
| 选项 | 实验内容 | 实验设计 |
| A | 从H2O2溶液制O2的残余物中分离出MnO2 | 将残余物过滤、烘干 |
| B | 除去NaCl溶液中含有的少量MgCl2 | 加入过量Ca(OH)2溶液,过滤 |
| C | 除去铁粉中含有的少量铜粉 | 加入过量稀盐酸,过滤 |
| D | 验证某溶液为稀盐酸 | 先测溶液的pH<7,再加入锌粒 |
| A. | A | B. | B | C. | C | D. | D |
7.下列对分子、原子的认识,正确的是( )
| A. | 原子是最小的粒子,不可再分 | |
| B. | 原子能构成分子,但不能直接构成物质 | |
| C. | 气体容易压缩,是因为气体分子变小了 | |
| D. | 当品红溶于水时,品红分子和水分子没有变成其它分子 |
4.下列实验现象描述正确的 是( )
| A. | 铁在空气中燃烧,火星四射 | |
| B. | 镁在空气中燃烧,发出耀眼白光 | |
| C. | 氢氧化钠溶液和硫酸铜溶液混合生成紫色沉淀 | |
| D. | 蘸有浓盐酸和浓氨水的小团棉花靠近,两团棉花中间产生白雾 |
5. 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
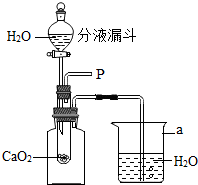
(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如右图所示的装置进行实验,打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是氧气.由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是补充鱼塘中的氧气,仪器a的名称是烧杯.
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物.开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2.请解释小强否定原假设建立新假设的理由:在水较多的环境中即使生成CaO,也会和水作用生成Ca(OH)2.
请设计一个实验方案来验证小强的新假设,并填入如表空格中:
(3)小强通过实验证明了过氧化钙与水反应的确有氢氧化钙生成,请写出过氧化钙和水反应的化学方程式:2CaO2+2H2O=2Ca(OH)2+O2↑.
(4)小强在实验时观察到烧杯中有气泡产生,由此他还得出了什么结论CaO2与H2O的反应是放热反应.
 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如右图所示的装置进行实验,打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是氧气.由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是补充鱼塘中的氧气,仪器a的名称是烧杯.
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物.开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2.请解释小强否定原假设建立新假设的理由:在水较多的环境中即使生成CaO,也会和水作用生成Ca(OH)2.
请设计一个实验方案来验证小强的新假设,并填入如表空格中:
| 实验步骤 | 可能出现的现象 | 结论 |
| 取反应后所得的溶液样品滴入酚酞指示剂(或通入CO2 气体) | 变红(或产生白色浑浊) | CaO2与H2O反应有Ca(OH)2生成 |
| / | CaO2与H2O反应无Ca(OH)2生成 |
(4)小强在实验时观察到烧杯中有气泡产生,由此他还得出了什么结论CaO2与H2O的反应是放热反应.
 A、B、C、D分别是初中常见的物质,且都含有氧元素,它们之间存在顺时针的转化关系,如图所示.若空气中A含量过多会造成温室效应,B是石灰石的主要成分,C是生活中常见的液态物质.
A、B、C、D分别是初中常见的物质,且都含有氧元素,它们之间存在顺时针的转化关系,如图所示.若空气中A含量过多会造成温室效应,B是石灰石的主要成分,C是生活中常见的液态物质.