题目内容
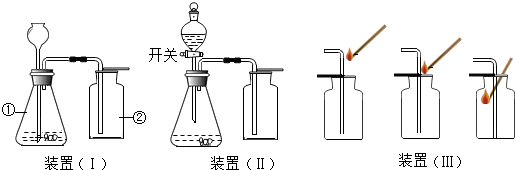
某除去杂质的实验操作中,为了将溶液中的杂质完全除去,通常需要加入过量的除杂质试剂.某校化学课外活动小组为了除去粗盐中含有的少量Na2SO4、MgCl2,设计了下列实验步骤:
试简要说明:
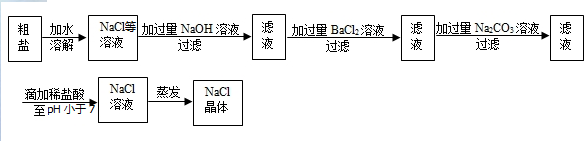
(1)加入NaOH的目的
(2)加入过量BaCl2溶液的原因
(3)加入过量Na2CO3溶液的原因
(4)加入盐酸为什么可以过量 .
试简要说明:

(1)加入NaOH的目的
(2)加入过量BaCl2溶液的原因
(3)加入过量Na2CO3溶液的原因
(4)加入盐酸为什么可以过量
考点:氯化钠与粗盐提纯,碱的化学性质,盐的化学性质
专题:常见的盐 化学肥料
分析:根据溶液中含有杂质、常见物质的性质分析加入物质的目的或原因.
解答:解:(1)由于溶液中含有镁离子,加入NaOH的目的使镁离子转化为沉淀而除去;
(2)由于溶液中含有硫酸根离子,加入过量BaCl2溶液的原因使硫酸根离子转化为沉淀而除去;
(3)在上述试验过程中加入了氯化钡,所以,加入过量Na2CO3溶液的原因使钡离子转化为沉淀而除去;
(4)由上述的试验程可知,溶液中含有过量的氢氧根离子、碳酸根离子.所以,加入盐酸为什么可以除去过量的氢氧根离子和 碳酸根离子,得到氯化钠,由于盐酸易挥发,可以过量.
故答为:(1)使镁离子转化为沉淀而除去;(2)使硫酸根离子转化为沉淀而除去;(3)使钡离子转化为沉淀而除去;(4)过量的盐酸在蒸发时可以挥发.
(2)由于溶液中含有硫酸根离子,加入过量BaCl2溶液的原因使硫酸根离子转化为沉淀而除去;
(3)在上述试验过程中加入了氯化钡,所以,加入过量Na2CO3溶液的原因使钡离子转化为沉淀而除去;
(4)由上述的试验程可知,溶液中含有过量的氢氧根离子、碳酸根离子.所以,加入盐酸为什么可以除去过量的氢氧根离子和 碳酸根离子,得到氯化钠,由于盐酸易挥发,可以过量.
故答为:(1)使镁离子转化为沉淀而除去;(2)使硫酸根离子转化为沉淀而除去;(3)使钡离子转化为沉淀而除去;(4)过量的盐酸在蒸发时可以挥发.
点评:本题属于物质的除杂,在除杂质时,一定要将引入的物质再除去.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中属于氧化物的是( )
| A、H2SO4 |
| B、CaO |
| C、NH4NO3 |
| D、NaOH |
下列认识或说法中,正确的是( )
| A、向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- |
| B、常温下可用Fe与HCl反应制取FeCl3 |
| C、可用燃烧的方法除去CO2中CO |
| D、分别将Mg、Fe、Cu放入稀盐酸中,可确定它们的活动性顺序 |
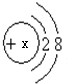 ,若X等于11,则该微粒表示
,若X等于11,则该微粒表示