题目内容
5.有A、B、C三种元素,A原子为质量最小的原子,B元素为地壳中含量最多的金属元素,C原于得到2个电子后与氖原子的电子层结构相同,由A、B、C元素中的一种、两种或三种元素组成的物质中,写出两种气态单质的化学式:H2、O2;写出两种化合物的化学式(是氧化物的在化学式后面标出)H2O氧化物、H2O2氧化物.分析 根据A、B、C三种元素,A原子为质量最小的原子,所以A是氢元素,B元素为地壳中含量最多的金属元素,所以B是铝元素,C原于得到2个电子后与氖原子的电子层结构相同,所以C是氧元素,然后将推出的元素进行验证即可.
解答 解:A、B、C三种元素,A原子为质量最小的原子,所以A是氢元素,B元素为地壳中含量最多的金属元素,所以B是铝元素,C原于得到2个电子后与氖原子的电子层结构相同,所以C是氧元素,经过验证,推导正确,所以两种气态单质的化学式为:H2、O2;两种化合物的化学式为:H2O氧化物,H2O2氧化物.
故答案为:H2、O2;H2O氧化物,H2O2氧化物.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
19.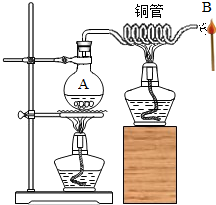 如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )
如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )
 如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )
如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )| A. | B处水蒸气对火柴起引燃作用 | |
| B. | 火柴移离水蒸气才能燃烧是因为水蒸气具有助燃性 | |
| C. | 把螺旋状的铜管拉成直线型,实验效果更显著 | |
| D. | 该实验只证明了可燃物的燃烧需要足够的氧气 |
6.需将质量分数为60%的蔗糖溶液用水稀释成质量分数为20%的蔗糖溶液,则蔗糖溶液与水混合的质量比应为( )
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 1:3 |
15. 科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
①选择装置并检查气密性.
②称取0.1g的二氧化锰粉末加入容器中.
③量取20毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
④改变二氧化锰的质量,重复上述实验,记录数据如表.
(1)本实验探究的问题是二氧化锰的质量对过氧化氢分解快慢的影响.从表中数据分析得出的结论是其他条件相同时,二氧化锰的质量越大反应速率越快.
(2)写出实验室用过氧化氢溶液制取氧气反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)对于有气体生成的反应,要准确比较反应速率的快慢,除上述方法外,你还可以采用的方法是比较收集相同体积的气体所需时间的长短.
(4)为了完成本实验应选用的收集装置是③.(填序号)
(5)对于催化剂对化学反应速率的影响还有哪些因素,你可以大胆提出猜想,并设计实验进行验证.(要求仍以过氧化氢分解为例)
你的猜想:催化剂的种类不同影响过氧化氢分解的速率.
你的实验设计:(要有实验操作步骤、现象和结论)
步骤:在常温下,①分别称取0.1g的红砖粉末和二氧化锰加入到大试管内;②分别向大试管中加入20mL5%的过氧化氢溶液;③用排水法分别收集一瓶氧气并记录所需的时间
现象和结论:放入二氧化锰收集一瓶氧气所需的时间比放入红砖粉末的短,说明二氧化锰的催化效果比红砖粉末要好.
 科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.①选择装置并检查气密性.
②称取0.1g的二氧化锰粉末加入容器中.
③量取20毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
④改变二氧化锰的质量,重复上述实验,记录数据如表.
| 时间/秒 | 生成氧气的体积/毫升 | |||
| 0.1g MnO2 | 0.2g MnO2 | 0.3g MnO2 | 0.4g MnO2 | |
| 40 | 49 | 61 | 75 | 86 |
| 80 | 77 | 87 | 90 | 92 |
| 120 | 89 | 92 | 92 | 92 |
| 160 | 92 | 92 | 92 | 92 |
(2)写出实验室用过氧化氢溶液制取氧气反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)对于有气体生成的反应,要准确比较反应速率的快慢,除上述方法外,你还可以采用的方法是比较收集相同体积的气体所需时间的长短.
(4)为了完成本实验应选用的收集装置是③.(填序号)
(5)对于催化剂对化学反应速率的影响还有哪些因素,你可以大胆提出猜想,并设计实验进行验证.(要求仍以过氧化氢分解为例)
你的猜想:催化剂的种类不同影响过氧化氢分解的速率.
你的实验设计:(要有实验操作步骤、现象和结论)
步骤:在常温下,①分别称取0.1g的红砖粉末和二氧化锰加入到大试管内;②分别向大试管中加入20mL5%的过氧化氢溶液;③用排水法分别收集一瓶氧气并记录所需的时间
现象和结论:放入二氧化锰收集一瓶氧气所需的时间比放入红砖粉末的短,说明二氧化锰的催化效果比红砖粉末要好.
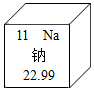 如图是元素周期表中的一格.钠的相对原子质量为22.99,其原子结构示意图为
如图是元素周期表中的一格.钠的相对原子质量为22.99,其原子结构示意图为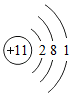 ,该元素在元素周期表中位于第三周期的最左边(填“最左边”、“中间”或“最右边”).
,该元素在元素周期表中位于第三周期的最左边(填“最左边”、“中间”或“最右边”).
 小明同学发现他家菜园中的蔬菜生长迟缓发黄,他联系自己学过的生物知识估计到是缺氮肥了,于是就到农资商店去咨询购买,他发现商店里一种化肥的包装袋上的标签如图,请同学们帮计算:
小明同学发现他家菜园中的蔬菜生长迟缓发黄,他联系自己学过的生物知识估计到是缺氮肥了,于是就到农资商店去咨询购买,他发现商店里一种化肥的包装袋上的标签如图,请同学们帮计算: