题目内容
12.在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用.如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:
(1)食用“碘盐”属于混合物(纯净物或混合物)
(2)碘酸钾(KIO3)中钾元素、碘元素的质量比是39:127.
(3)碘酸钾(KIO3)中碘元素的质量分数是59.3%.(计算结果精确到0.1%)
(4)一袋净重500g的上述碘盐至少含0.01g碘元素,折合碘酸钾0.168g.
分析 (1)根据混合物的定义进行分析;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
(3)物质中 某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{化合物的相对分子质量}$×100%,进行解答;
(4)根据题中信息:含碘量(20-30)mg/kg,即可计算成人至少补充碘元素.
解答 解:(1)食用“碘盐”是由氯化钠和碘酸钾组成的,属于混合物;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,可得碘酸钾(KIO3)中钾元素、碘元素的质量比为:39:127;
(3)物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{化合物的相对分子质量}$×100,可得碘酸钾(KIO3)中碘元素的质量分数=$\frac{127}{127+39+16×3}$×100%=59.3%;
(4)根据题中信息:含碘量(20-30)mg/kg,可知一袋净重500g的上述碘盐至少含碘元素质量为:500g×$\frac{20mg}{1000g}$=1mg=0.01g,折合碘酸钾质量为:$\frac{0.01g}{59.3%}$=0.168g.
故答案为:(1)混合物;
(2)39:127;
(3)59.3%;
(4)0.01g,0.168g.
点评 本题考查学生根据物质化学式分析元素质量比,及对化合物中元素的质量分数计算方法的掌握与与在解题中应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.如图为配置50g溶质质量分数为10%的氯化钠溶液的操作过程,下列有关操作与目的分析均正确的是( )
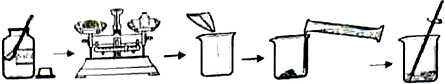

| 选项 | 操作 | 目的 |
| A | 用剩的食盐放回原试剂瓶 | 避免浪费 |
| B | 天平调平后在左、右托盘中各垫一张相同的纸 | 保证称取的食盐质量更准确 |
| C | 用50ml量筒替代天平量取所需的水 | 更加简便 |
| A. | A | B. | B | C. | C |
16.一瓶氢氧化钠溶液因密封不好已部分发生变质,如要除去杂质,使其重新变成氢氧化钠,可加入适量的( )
| A. | 稀盐酸 | B. | 氯化钙溶液 | C. | 澄清石灰水 | D. | 氯化钠溶液 |
4.下来有关实验基本操作,正确的是( )
| A. |  点燃酒精灯 | B. |  取用固体粉末 | C. |  塞紧橡皮塞 | D. |  闻气体气味 |
1.除去下列物质中混有的少量杂质,所选用的试剂及操作方法错误的是( )
| 序号 | 物质 | 杂质(少量) | 除去杂质的方法 |
| A | O2 | 水蒸气 | 通过生石灰 |
| B | C粉 | 氧化铜 | 加入过量稀盐酸,过滤 |
| C | 氯化钙溶液 | 稀盐酸 | 加入过量氢氧化钙溶液,过滤 |
| D | NaCl溶液 | Na2CO3 | 加入稀硫酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
2.在H2O、H2O2、H2SO4三种分子中都含有( )
| A. | 氢气 | B. | 氢原子 | C. | 氢分子 | D. | 氢元素 |
 A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,各物质间存在如下转化关系(反应的条件已省略):
A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,各物质间存在如下转化关系(反应的条件已省略):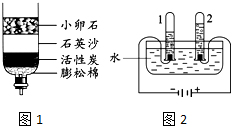 水是重要的资源.
水是重要的资源.