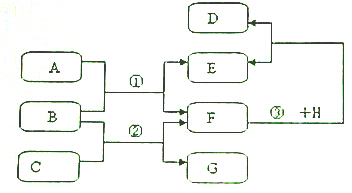
题目内容
7.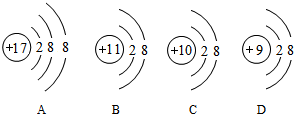 根据下列粒子结构示意图,回答问题:
根据下列粒子结构示意图,回答问题:(1)A粒子核外电子层数为3,该粒子带1个单位的负电荷.
(2)属于阳离子的是B(填字母,下同);属于原子的是C.
(3)核外电子数相同的是BCD.
(4)若钠的相对原子质量为23,其质子数为11,则其原子核内中子数为12.
分析 (1)粒子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,据此进行分析解答.
(2)当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
(3)根据四种粒子的核外电子数进行分析解答.
(4)根据相对原子质量=质子数+中子数,进行分析解答.
解答 解:(1)弧线表示电子层,A粒子的核外电子层数为3;该粒子质子数=17,核外电子数=18,质子数<核外电子数,为带1个单位负电荷的阴离子.
(2)B质子数=11,核外电子数=10,质子数>核外电子数,为阳离子;C质子数=核外电子数=10,为原子.
(3)由粒子结构示意图,BCD的核外电子数相同,均为10.
(4)相对原子质量=质子数+中子数,钠的相对原子质量为23,其质子数为11,则其原子核内中子数为23-11=12.
故答案为:(1)3;1;负;(2)B;C;(3)BCD;(4)12.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
10.铝热法是一种利用铝 的还原性获得高熔点的金属 单质的方法,可简单地认为是铝与某些金属在高温条件下发生的化学反应,如:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,该反应所属的基本反应类型为( )
| A. | 化合反应 | B. | 分解反应 | C. | 复分解反应 | D. | 置换反应 |
8.绿色化学就是从源头上消除对环境的污染,下列措施不符合绿色化学理念的是( )
| A. | 积极发展太阳能产业 | |
| B. | 增加燃煤火力发电厂 | |
| C. | 降低化石能源在能源结构中的比例 | |
| D. | 加强氢能源的开发利用已知反应前后分子变化 |
12.t1℃时,分别将20g甲、乙两种晶体(不含结晶水)加入盛有100g水的两个烧杯中,恰好完全溶解,升温到t2℃时出现甲、乙烧杯中所示图1的现象.根据上述实验,结合如图2中甲、乙两物质的溶解度曲线,判断下列说法不正确的是(改编)( )


| A. | t1℃时烧杯中甲、乙两物质形成的溶液是饱和溶液 | |
| B. | t1℃时烧杯中甲的溶液溶质质量分数约为16.7% | |
| C. | t2℃时烧杯中甲物质溶液的质量是115g | |
| D. | 甲物质可能是氢氧化钙 |
16.某两种物质在光照条件下能发生化学反应,其意图如下,则下列说法中正确的是( )
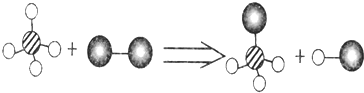 (说明:一种小球代表一种元素的原子)
(说明:一种小球代表一种元素的原子)
 (说明:一种小球代表一种元素的原子)
(说明:一种小球代表一种元素的原子)| A. | 图示中的反应物都是单质 | B. | 该反应属于化合反应 | ||
| C. | 图示中共有4 种物质 | D. | 该反应属于置换反应 |
17.下图是实验室二氧化碳的制取、收集、验满、验证性质的操作,其中不正确的是( )
| A. | 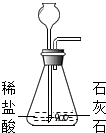 制取 | B. | 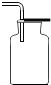 收集 | C. | 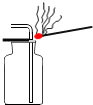 验满 | D. | 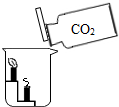 检验性质 |