题目内容
10.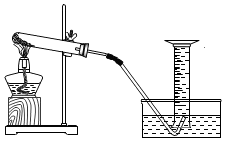 在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验,老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组.
在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验,老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组.(1)结合老师建议,补充完整实验步骤①之后的其它步骤,①检查装置的气密性;
…
(2)实验结束后,小明回收了二氧化锰,如果要证明二氧化锰是氯酸钾分解的催化剂,还需验证二氧化锰的质量和化学性质保持不变.
分析 (1)根据老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组进行设计并补充实验步骤;
(2)根据催化剂的定义:在化学反应中,改变化学反应速率,而本身的质量和化学性质在反应前后都不变进行分析.
解答 解:(1)通过分析实验设计的要求,①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组,可知
①检查装置的气密性;
②取4克的氯酸钾与0.5克二氧化锰,均匀混合后加入试管中,连接好装置;
③开始加热试管,用秒表记录量筒收集一定体积氧气的时间;
④换用三支相同的试管,各加入4克氯酸钾,分别于1克、1.5克、2克的二氧化锰均匀混合,用相同装置重复步骤②③;
⑤比较实验记录的四次时间大小,判断氯酸钾的分解速率与二氧化锰用量的关系.
(2)实验结束后,小明回收了二氧化锰,如果要证明二氧化锰是氯酸钾分解的催化剂,还需验证二氧化锰的质量和化学性质保持不变.
故答案为:(1)②取4克的氯酸钾与0.5克二氧化锰,均匀混合后加入试管中,连接好装置;
③开始加热试管,用秒表记录量筒收集一定体积氧气的时间;
④换用三支相同的试管,各加入4克氯酸钾,分别于1克、1.5克、2克的二氧化锰均匀混合,用相同装置重复步骤②③;
⑤比较实验记录的四次时间大小,判断氯酸钾的分解速率与二氧化锰用量的关系.
(2)质量和化学性质.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
8.人体健康与化学关系密切,下列叙述错误的是( )
| A. | 纤维素是构成植物细胞的基础物质,不能被人体消化,蔬菜和粗粮等含纤维素较多 | |
| B. | 青少年缺锌会引起生长迟缓,发育不良,可适当食用海产品、奶类、小米等食物 | |
| C. | 为减轻蚊虫叮咬后的痛痒感,可涂抹牙膏、肥皂水等 | |
| D. | 维生素有20多种,多数在人体内不能合成,缺乏维生素C,会引起夜盲症 |
1.下列有关实验操作中无安全隐患的是( )
| A. | 桌子上酒精燃烧,用水扑灭 | |
| B. | 用高锰酸钾制取氧气结束后,先熄灭酒精灯,再从水槽中撤离导管 | |
| C. | 鉴别实验室的食盐和白糖,用品尝的方法 | |
| D. | 待试管冷却后,再用清水冲洗试管 |
18.除去下列物质中混有的少量杂质(括号内为杂质),所用试剂和方法不正确的是( )
| A. | N2中的(O2 ) 红热的木炭 | |
| B. | NaCl溶液中的(Na2CO3) 加入稀盐酸 | |
| C. | FeCl2溶液中的(CuCl2) 加入过量铁粉,过滤 | |
| D. | 铜粉中的(铁) 加入过量稀硫酸,过滤 |
5.如图是元素周期表中铁、氧两种元素的相关信息,下列有关说法正确的是( )
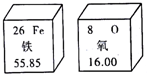

| A. | 氧原子的核外电子数为8 | |
| B. | 铁元素和氧元素都属于非金属元素 | |
| C. | 铁的相对原子质量是55.85g | |
| D. | 铁元素与氧元素只能组成一种化合物 |
15.溶液在日常生活中应用广泛.下列对溶液的有关说法正确的是( )
| A. | 溶液都是无色、透明的液体 | |
| B. | 溶液中不能同时存两种溶质 | |
| C. | 溶液中各部分密度不同 | |
| D. | 外界条件不改变,溶质溶剂不会分离 |
20.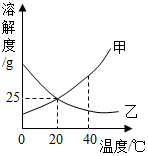 如图所示为甲、乙固体的溶解度曲线,下列说法错误的是( )
如图所示为甲、乙固体的溶解度曲线,下列说法错误的是( )
 如图所示为甲、乙固体的溶解度曲线,下列说法错误的是( )
如图所示为甲、乙固体的溶解度曲线,下列说法错误的是( )| A. | 40℃时,甲的溶解度大于乙的溶解度 | |
| B. | 20℃时,甲、乙两种物质的溶解度相等 | |
| C. | 甲、乙两种物质的溶解度都随温度的升高而增大 | |
| D. | 20℃时,把30g甲物质加入100g水中,充分溶解后所得溶液为饱和溶液 |


