题目内容
2.下列图象不能正确反应其对应关系的是( )| A. | 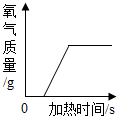 加热一定量的高锰酸钾 | |
| B. | 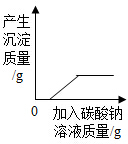 向含有HCl和CaCl2的混合溶液中加入Na2CO3溶液 | |
| C. | 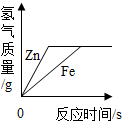 向等质量等质量分数的稀盐酸中分别加入过量的锌和铁 | |
| D. | 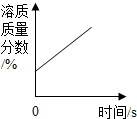 将一瓶浓硫酸敞口放置在空气中 |
分析 A、根据加热一定量的高锰酸钾固体,氧气质量不断增加,当反应完毕后氧气质量不再增加为一定值进行解答;
B、根据碳酸钠优先于盐酸反应进行解答;
C、根据在金属活动性顺序中,位置越靠前的金属与酸反应的速率越快分析.
D、根据浓硫酸具有吸水性,敞口放置在空气中溶质质量分数减小分析.
解答 解:A、加热一定量的高锰酸钾固体,氧气质量不断增加,当反应完毕后氧气质量不再增加为一定值,并且开始加热时温度达不到,不会分解,不能生成气体,故正确;
二氧化锰做催化剂,反应前后质量不变,故A错误;
B、加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了,故起始无沉淀.故正确;
C、在金属活动性顺序中,锌>铁,锌与酸反应生成氢气的速率大于铁;同时因金属足量,相同质量的酸液完全反应生成氢气的质量相等,故正确;
D、浓硫酸具有吸水性,敞口放置在空气中溶质质量分数减小,图象不能正确反映其对应关系.
故选:D
点评 本题是结合图象的分析题,解题时注意分析清楚转折点即可较快做出判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列气体中,即能用浓硫酸干燥,又能用固体氢氧化钠干燥的是( )
| A. | CO2 | B. | SO2 | C. | H2 | D. | NH3 |
17.下列实验现象的描述中,不正确的是( )
| A. | 细铁丝在氧气中燃烧,火星四射,产生黑色固体 | |
| B. | 将氢氧化钠溶液滴入氯化铁溶液中,有红褐色沉淀产生 | |
| C. | 将二氧化碳通入紫色石蕊溶液中,溶液变为蓝色 | |
| D. | 将(NH4)2SO4和熟石灰混合研磨,有刺激性气味产生 |
7.如图是模拟海水制盐的流程
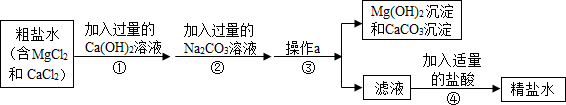
(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若无白色沉淀产生(填实验现象),则证明Ca(OH)2溶液已过量.
(2)实验结束后,兴趣小组对滤液进行探究
【提出问题】滤液中除了含有水和氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有氢氧化钠 和碳酸钠.
【验证猜想】
【实验结论】经过兴趣小组的实验分析,推出猜想三是正确的.
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O或Na2CO3+2HCl═2NaCl+H2O+CO2↑.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶 操作.
【定量计算】若用上述NaCl晶体配置溶液,取一定质量的该溶液加入足量的AgNO3溶液,所得AgCl沉淀质量等于原NaCl溶液质量.请计算原NaCl溶液中溶质的质量分数.

(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若无白色沉淀产生(填实验现象),则证明Ca(OH)2溶液已过量.
(2)实验结束后,兴趣小组对滤液进行探究
【提出问题】滤液中除了含有水和氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有氢氧化钠 和碳酸钠.
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 推断 |
| 1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | 有白色沉淀生成 | 滤液中还含有碳酸钠 溶质 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入 无色酚酞试液 (填指示剂) | 溶液变红色 | 滤液中还含有氢氧化钠 |
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O或Na2CO3+2HCl═2NaCl+H2O+CO2↑.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶 操作.
【定量计算】若用上述NaCl晶体配置溶液,取一定质量的该溶液加入足量的AgNO3溶液,所得AgCl沉淀质量等于原NaCl溶液质量.请计算原NaCl溶液中溶质的质量分数.
14.下列有关概念的辨析中正确的是( )
| A. | 一种元素只能组成一种单质 | |
| B. | 原子不能保持物质的化学性质 | |
| C. | 带有电荷的微粒可能不是离子 | |
| D. | 元素的种类是由原子的最外层电子数决定的 |
12.下列实验现象描述错误的是( )
| A. | 铁丝在氧气中燃烧火星四射 | |
| B. | 硫在氧气中燃烧产生蓝紫色火焰 | |
| C. | 红磷在氧气中燃烧产生白雾 | |
| D. | 铁丝浸入硫酸铜溶液表面有红色物质生成 |