题目内容
5.将一定量的木炭和氧气置于一个封闭的容器中灼烧点燃,测得反应前后各物质的质量如表:| 物质 | 木炭 | 氧气 | 二氧化碳 | X |
| 反应前质量/g | 2.4 | 4.8 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | a |
| A. | 表中a的值为2.8g | |
| B. | 该反应不遵守质量守恒定律 | |
| C. | X是该反应的催化剂 | |
| D. | 无论如何改变氧气的起始量,均有X生成 |
分析 本题考查的是质量守恒定律,其内容是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,先根据质量守恒定律计算a的值,然后判断X是否是催化剂;所有的化学变化都遵守质量守恒定律.
解答 解:A、根据质量守恒定律可知,a=2.4+4.8-4.4=2.8,故说法正确.
B、所有的化学变化都遵守质量守恒定律,故选项错误.
C、X反应后质量增加,属于生成物,故选项错误.
D、氧气足量时只有二氧化碳生成,因此增加氧气的起始量,就没有X生成,故选项错误.
故选A.
点评 本考点是有关质量守恒定律的探究,属于表格型信息题,有关质量守恒定律的考题在中考中经常出现,要抓住要点,难度不大.

练习册系列答案
相关题目
1.如表是元素周期表的一部分,请根据表中提供的信息按要求填空.
(1)元素①是Al(填元素符号);由6、8、11号三种元素组成的物质化学式为Na2CO3.
(2)由元素②组成的单质在空气中燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)请画出原子序数是9的元素的原子结构示意图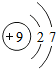 ,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).
,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).
(4)在元素周期表中,同一周期的元素最外层电子数的变化规律是:从左到右随着核电荷数的依次递增最外层电子数依次增多.
| 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 11 Na 镁 | 12 Mg 镁 | ① | 14 Si 硅 | ② | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |
(2)由元素②组成的单质在空气中燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)请画出原子序数是9的元素的原子结构示意图
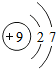 ,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).
,化学反应中该元素的原子易得到电子(填“得到”或“失去”),形成阴离子(填“阴”或“阳”).(4)在元素周期表中,同一周期的元素最外层电子数的变化规律是:从左到右随着核电荷数的依次递增最外层电子数依次增多.
2.下列说法错误的是( )
| A. | 铁丝在氧气中燃烧有黑色固体生成 | |
| B. | 浓硫酸可做干燥剂是因为浓硫酸具有脱水性 | |
| C. | 废水中含有酸性物质必须先用碱性物质中和成中性以后才能排放 | |
| D. | 石墨质软滑腻,能导电、导热、耐高温 |
10.如果把家庭中的①食盐 ②纯碱(碳酸钠) ③白醋 ④芝麻油 ⑤蔗糖⑥面粉 ⑦白酒分别放入适量水中充分搅拌,能够形成溶液的是( )
| A. | ①③⑤⑦ | B. | ①②⑤⑥ | C. | ①②③⑥ | D. | ①②③⑤⑦ |