题目内容
2.如图所示装置可以验证某混合气体中(无色无味)是否含有CO2和CO,请回答下列问题:(提示:氢氧化钠溶液和澄清石灰水的化学性质相似,氢氧化钠溶液吸收二氧化碳的能力比澄清石灰水强)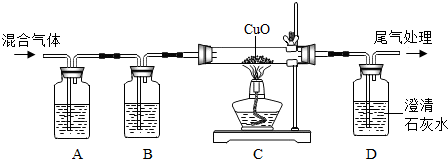
(1)A装置中的试剂足(写名称,下同)澄清石灰水,B装置中的试剂是氢氧化钠溶液.
(2)证明原混合气体中CO2存在的实验现象是A中澄清石灰水变浑浊;证明原混合气体中CO存在的实验现象是C中黑色粉末变红,D中澄清石灰水变浑浊.
(3)如果没有B装置,对实验结果有何影响?没有B装置,无法除掉CO2,从而无法判断原混合气体中是否含有CO气体.
(4)写出C和D中的化学方程式CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2,Ca(OH)2+CO2=CaCO3↓+H2O.
(5)若取20g高锰酸钾防入试管中,加热一段后,固体质量减少1.6g.请计算试管中剩余高锰酸钾的质量.
分析 使澄清石灰水变浑浊是CO2的特性,所以装置A中的试剂为澄清石灰水;验证CO往往是验证其与氧化铜反应后有无CO2生成,但在与氧化铜反应之前,应把混合气体中的CO2完全除净,否则将无法证明反应后所含有的CO2是反应生成的,还是反应前就有的,所以装置B中盛放的应能吸收CO2的NaOH溶液.
根据高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,可知由于氧气的放出而使加热一段时间后试管内固体质量减少,因此固体减少的质量就是生成的氧气的质量,然后利用反应中各物质的质量关系计算出试管中剩余高锰酸钾的质量.
解答 解:(1)使澄清石灰水变浑浊是CO2的特性,装置A是用来检验二氧化碳的,故A中的试剂为澄清石灰水;B装置是用来吸收二氧化碳的,故应为氢氧化钠溶液;
(2)证明原混合气体中CO2存在的实验现象是A中澄清石灰水变浑浊;证明原混合气体中CO存在的实验现象是C中黑色粉末变红,D中澄清石灰水变浑浊,注意两种现象缺一不可;
(3)验证CO往往是验证其与氧化铜反应后有无CO2生成,但在与氧化铜反应之前,应把混合气体中的CO2完全除净,否则将无法证明反应后所含有的CO2是反应生成的,还是反应前就有的,故没有B装置,无法除掉CO2,从而无法判断原混合气体中是否含有CO气体.
(4)C中是一氧化碳与氧化铜反应生成铜和二氧化碳;D中是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;
(5)固体质量减少了1.6g,就是生成的氧气的质量.
解:设剩余高锰酸钾的质量为x.
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
20g-x 1.6g
$\frac{316}{20g-x}=\frac{32}{1.6g}$
x=4.2g
故答案为:(1)澄清石灰水,氢氧化钠溶液;
(2)A中澄清石灰水变浑浊;C中黑色粉末变红,D中澄清石灰水变浑浊;
(3)没有B装置,无法除掉CO2,从而无法判断原混合气体中是否含有CO气体.
(4)CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2; Ca(OH)2+CO2=CaCO3↓+H2O.
(5)剩余高锰酸钾的质量为4.2g.
点评 此题主要是考查同学们的综合分析能力,不但要求同学们具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

| A. | 纯铁具有明亮的红色光泽,质硬,延展性好 | |
| B. | 生铁是含杂质较多的铁合金 | |
| C. | 铁器表面涂上油漆的目的只是为了美观 | |
| D. | 铁在潮湿的空气中容易生锈 |
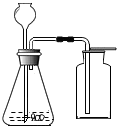 利用下列方法制备气体时:①石灰石和稀盐酸制取二氧化碳;②锌和稀硫酸制取氢气;③过氧化氢的水溶液和二氧化锰制取氧气;④氯酸钾和二氧化锰加热制取氧气,可以采用右图所示装置制备和收集气体的是( )
利用下列方法制备气体时:①石灰石和稀盐酸制取二氧化碳;②锌和稀硫酸制取氢气;③过氧化氢的水溶液和二氧化锰制取氧气;④氯酸钾和二氧化锰加热制取氧气,可以采用右图所示装置制备和收集气体的是( )| A. | ①②② | B. | ⑨③ | C. | ①②③④ | D. | ①③ |
 如图是镁原子的原子结构示意图,下列对镁原子的叙述不正确的是( )
如图是镁原子的原子结构示意图,下列对镁原子的叙述不正确的是( )| A. | 镁原子第二电子层有8个电子 | |
| B. | 镁原子最外层电子的能量低于第二层电子的能量 | |
| C. | 镁原子核内有12个质子 | |
| D. | 镁原子在化学反应中容易失去电子 |
(1)[猜想]
①小新猜想:活动性X大于Y ②小米猜想:活动性Y大于X
(2)[设计方案并进行实验]完成好如下实验报告,并回答后续有关问题.
| 实验步骤 | 实验现象 | 结论 |
| 金属Y表面无明显变化;金属X的表面有大量气泡冒出.将燃着的木条放在金属X的试管口,气体燃烧. | 小新的猜想: 正确(“正确”或“不正确”) |
(4)小米向Zn(NO3)2、AgNO3、Cu(NO3)2混合溶液中加入一些X,完全反应后过滤.取滤渣于试管中,加稀盐酸,有气体生成.则滤液中的溶质是硝酸锌和硝酸亚铁.
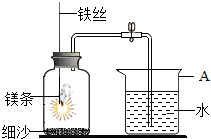 小强同学为了探究空气中氧气的体积分数,设计了如图所示的实验:镁条在空气中燃烧,当燃烧停止、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.请回答:
小强同学为了探究空气中氧气的体积分数,设计了如图所示的实验:镁条在空气中燃烧,当燃烧停止、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.请回答: