题目内容
【题目】为测定某纯碱样品![]() 杂质为氯化钠
杂质为氯化钠![]() 中碳酸钠的含量,某小组同学进行了如图所示的实验,请回答问题:
中碳酸钠的含量,某小组同学进行了如图所示的实验,请回答问题:
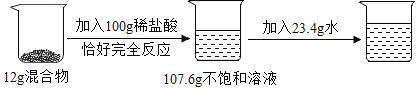
![]() 写出反应的化学方程式______;
写出反应的化学方程式______;
![]() 列出求解混合物中参加反应的物质质量
列出求解混合物中参加反应的物质质量![]() 的比例式______;
的比例式______;
![]() 样品中碳酸钠的含量为______
样品中碳酸钠的含量为______![]() 最终结果保留整数
最终结果保留整数![]() ;
;
![]() 最终所得溶液的溶质质量分数为______;
最终所得溶液的溶质质量分数为______;
![]() 若用质量分数
若用质量分数![]() 的浓盐酸配制实验所需稀盐酸,需要浓盐酸和水的质量比为______。
的浓盐酸配制实验所需稀盐酸,需要浓盐酸和水的质量比为______。
【答案】![]()
![]()
![]()
![]() 1:4
1:4
【解析】
(1)碳酸钠和氯化钠中只有碳酸钠和盐酸反应生成氯化钠和水以及二氧化碳,对应的化学方程式为![]() ;
;
(2)根据质量守恒定律可得,生成的二氧化碳的质量为![]() ;
;
设:生成的氯化钠的质量为y,碳酸钠的质量为x,HCl的质量为z。
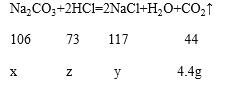
![]()
![]()
![]()
![]() ;
;
(3)该“碱”样品中碳酸钠的含量=![]() ;
;
(4)若最终得到的滤液为不饱和溶液,则所得滤液中溶质的质量分数=![]() ;
;
(5)若用![]() 的浓盐酸配制上述实验所用的稀盐酸,需浓盐酸的质量为
的浓盐酸配制上述实验所用的稀盐酸,需浓盐酸的质量为![]() ,水的质量为
,水的质量为![]() ,需要浓盐酸和水的质量比为20g:
,需要浓盐酸和水的质量比为20g:![]() :4。
:4。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目