题目内容
17.氧化钠常作漂白剂.它由钠离子和氧离子构成.(1)1个钠离子的化学符号是Na+.
(2)氧离子的结构示意图为
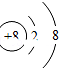 ,一个氧离子中有8个质子.
,一个氧离子中有8个质子.(3)氧化钠可以和水在常温下生成一种具有强烈腐蚀性的碱,请写出氧化钠与水反应的化学方程式Na2O+H2O═2NaOH.
分析 (1)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
(2)氧离子的结构示意图为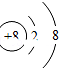 ,由圆圈内数字表示核内质子数,进行分析解答.
,由圆圈内数字表示核内质子数,进行分析解答.
(3)氧化钠可以和水在常温下生成一种具有强烈腐蚀性的碱,由质量守恒定律,反应前后元素种类不变,该碱是氢氧化钠,写出反应的化学方程式即可.
解答 解:(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.1个钠离子可表示为:Na+.
(2)氧离子的结构示意图为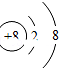 ,由圆圈内数字表示核内质子数,则一个氧离子中有8个质子.
,由圆圈内数字表示核内质子数,则一个氧离子中有8个质子.
(3)氧化钠可以和水在常温下生成一种具有强烈腐蚀性的碱,由质量守恒定律,反应前后元素种类不变,该碱是氢氧化钠,反应的化学方程式为Na2O+H2O═2NaOH.
故答案为:(1)Na+;(2)8;(3)Na2O+H2O═2NaOH.
点评 本题难度不大,掌握常见化学用语(粒子结构示意图、化学方程式、离子符号等)的书写方法正确解答此类题的关键.

练习册系列答案
相关题目
7.物质的性质决定其用途.对下列物质性质与其对应用途的描述不相符的是( )
| A. | 铁导热性良好,可制铁锅 | B. | 氢气有还原性,可用于冶炼金属 | ||
| C. | 石墨质软,可作电极 | D. | 浓硫酸有吸水性,可作干燥剂 |
5.果醋是集营养、保健、食疗等功能为一体的新型饮品.以下制作过程中涉及化学变化的是( )
| A. | 洗净水果 | B. | 水果切片 | C. | 放入容器 | D. | 加冰糖、白醋酿造 |
12.“水是生命之源”,下列关于水的说法正确的是( )
| A. | 为了保护水资源,应禁止使用农药、化肥 | |
| B. | 通过电解水的实验证明,水是由氢元素和氧元素组成的 | |
| C. | 保持水的化学性质的最小粒子是氢原子和氧原子 | |
| D. | 水在常温下不能与二氧化碳发生反应 |
9.2016年第31届夏季奥运会即将在巴西顺利召开,本届奥运会部分建筑和物品如下:
(1)上述物品使用的金属材料是奖牌,有机合成材料是吉祥物.(填写一种)
(2)关于金银铜化学性质说法正确的是BC(填字母序号)
A.均可以被空气中氧气氧化 B.化学性质依次逐渐活泼
C.均可以导电 D.均可以和稀硫酸反应
(3)写出一个表现银铁两金属活泼性差异反应方程式Fe+2AgNO3=Fe(NO3)2+2Ag.
| 实物图片 |  |  |  |  |
| 名称 | 奖牌 | 吉祥物 | 火炬 | 主会场 |
| 材料 | 黄金、白银、紫铜 | PU皮、化纤填充物 | 丙烷燃料 | 钢筋混凝土 |
(2)关于金银铜化学性质说法正确的是BC(填字母序号)
A.均可以被空气中氧气氧化 B.化学性质依次逐渐活泼
C.均可以导电 D.均可以和稀硫酸反应
(3)写出一个表现银铁两金属活泼性差异反应方程式Fe+2AgNO3=Fe(NO3)2+2Ag.
6.下列离子在pH=2的溶液中能大量共存且溶液是无色的是( )
| A. | K+、SO42-、Cl- | B. | OH-、CO32-、Ca2+ | C. | Na+、SO42-、OH-- | D. | Na+、Cu2+、NO3- |
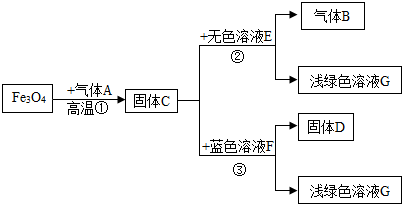 根据如图所示,回答下列问题(反应①、②、③均为完全反应).
根据如图所示,回答下列问题(反应①、②、③均为完全反应).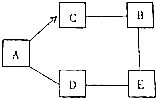 A~E为初中化学常见的五种物质,其类别各不相同,它们相互间的关系如图所示(“→”表示转化关系,“-”表示相互之间会反应).已知A是胃酸中含有的一种酸,C是氧化物,E的溶液呈蓝色.A、B、C、D、E的相对分分数依次增大.(部分反应物、生成物及反应条件已略去)
A~E为初中化学常见的五种物质,其类别各不相同,它们相互间的关系如图所示(“→”表示转化关系,“-”表示相互之间会反应).已知A是胃酸中含有的一种酸,C是氧化物,E的溶液呈蓝色.A、B、C、D、E的相对分分数依次增大.(部分反应物、生成物及反应条件已略去)