题目内容
7.现有两瓶无标签的澄清无色的液体,一瓶是室温下饱和的NaCl溶液,一瓶是纯净水,下列是905班级的探究小组的同学提供的鉴别方法和结论.其中正确的是( )①用高倍光学显微镜观察,能观察到两种微粒的是NaCl溶液;
②用AgNO3试剂检验,有白色固体出现的是NaCl溶液;
③称一称,比较轻的是纯净水;
④通电试验,容易导电的是纯净水;
⑤分别浸入新鲜菜柄,引起菜柄萎缩的是NaCl溶液;
⑥加热蒸发有白色固体出现的是NaCl溶液;
⑦用酚酞试液检验,变红色的是NaCl溶液.
| A. | ①②③ | B. | ②⑤⑥ | C. | ②③⑤ | D. | ②④⑥ |
分析 根据氯化钠和蒸馏水性质的不同进行逐项分析判断即可.
解答 解;①用高倍光学显微镜观察,不能能观察到两种微粒,故错误;
②氯化钠与硝酸银反应生成氯化银白色沉淀,因此用AgNO3试剂检验,有白色固体出现的是NaCl溶液,故正确;
③氯化钠溶液的密度比水大,相同体积的氯化钠溶液和纯净水,氯化钠溶液质量大,故正确;
④通电试验,容易导电的是氯化钠溶液,故错误;
⑤氯化钠溶液能使新鲜蔬菜渗出水分,因此分别浸入新鲜菜柄,引起菜柄萎缩的是NaCl溶液,故正确;
⑥氯化钠溶液中溶解氯化钠,因此加热蒸发有白色固体出现的是NaCl溶液,故正确;
⑦氯化钠溶液和蒸馏水都显中性,都不能使酚酞试液变红,故错误;
其中正确的是②③⑤⑥,观察选项正确的是B;
故选项为:B.
点评 我们在区分物质时通常是先从物理性质例如颜色、状态、气味、溶解性等方面来区分,然后再考虑它们的化学特性,利用相应的化学反应来进行鉴别.

练习册系列答案
相关题目
9. 如图是某元素的相关信息,下列说法正确的是( )
如图是某元素的相关信息,下列说法正确的是( )
 如图是某元素的相关信息,下列说法正确的是( )
如图是某元素的相关信息,下列说法正确的是( )| A. | 该元素为金属元素,相对原子质量为40.08g | |
| B. | 该元素的原子易失去两个电子形成阳离子,离子符号为Ca+2 | |
| C. | 该元素的离子其原子核内有20个质子 | |
| D. | 该元素的原子化学性质与He相似 |
15.下列关于说法正确的是( )
| A. | 水是由氢气和氧气组成的 | |
| B. | 化学变化中元素种类和原子个数均未发生变化 | |
| C. | 原子是化学变化中的最小粒子,因此原子是不可再分的实心球体 | |
| D. | 没有催化剂就不能进行化学反应 |
19.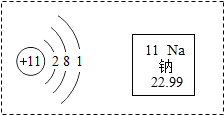 元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:它是的质子数是5或它的相对原子质量为10.81等.
(2)不同元素的本质区别是A
A.质子数 B.电子数 C.中子数 D.相对原子质量
(3)如图是钠原子的结构示意图,判断该原子容易失去(填“得到”或“失去”)电子,钠离子的符号为Na+.
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是b、d(填标号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水(H2O),用化学式表示该反应4HF+SiO2=SiF4+2H2O.
 元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:| 族 周期 | I A | II A | IIIA | IVA | VA | VIA | VIIA | 0 |
| 3 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)不同元素的本质区别是A
A.质子数 B.电子数 C.中子数 D.相对原子质量
(3)如图是钠原子的结构示意图,判断该原子容易失去(填“得到”或“失去”)电子,钠离子的符号为Na+.
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是b、d(填标号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水(H2O),用化学式表示该反应4HF+SiO2=SiF4+2H2O.