题目内容
下列是初中化学中的一些重要实验,请回答

(1)A是氢气或甲烷的燃烧实验,点燃前必须____________
(2)B实验中能够说明盐酸与氢氧化钠发生了反应的现象是________________________
(3)C是除去粗盐中难溶性杂质实验中的过滤操作,其中玻璃棒的作用是____________
(4)D是用碳酸钠粉末与稀盐酸反应制取二氧化碳的简易装置,此装置的最大优点是________________________________________________
【答案】(1)验纯 (2)溶液由红色变为无色(或红色消失)
(3)引流 (4)能够控制反应的速率(或能够控制反应的快慢)
【解析】(1)可燃性气体使用前必须要验纯;(2) 酚酞滴入氢氧化钠溶液中会变红,滴加稀盐酸后,氢氧化钠被反应掉,溶液不再显碱性,溶液由红色变为无色;(3)过滤时玻璃棒的作用是引流;(4)D装置可以通过控制滴加稀盐酸的速度来控制反应的速率。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案学习了CO2的有关知识后,同学们查阅资料发现Mg能在CO2中燃烧:CO2+2Mg C+2MgO。所以镁着火不能用CO2来灭火,但没有找到有关Na与CO2反应的介绍。于是同学们展开了钠着火能否用CO2来灭火的探究。
C+2MgO。所以镁着火不能用CO2来灭火,但没有找到有关Na与CO2反应的介绍。于是同学们展开了钠着火能否用CO2来灭火的探究。
【提出问题】钠能发生类似于CO2与镁的反应,可能的化学方程式为 。
【实验】将燃着的钠伸入装有CO2的集气瓶中,钠能在集气瓶中继续燃烧。
进一步【查阅资料】得知:
①Na2O是白色固体,能与CO2反应生成Na2CO3,也能与H2O反应生成NaOH.
②Ba (OH )2溶于水而BaCO3不溶于水。
③Na2CO3的存在会干扰NaOH的检测。
基于以上资料,同学们认为钠在CO2中燃烧的产物情况有所不同,并对产物提出了以下几种猜想:
I.Na2O、C;II. 、III.NaOH、C;IV.Na2O、Na2CO3、C
通过理论分析,猜想 (填序号)肯定是错误的,理由是 。
(验证猜想)
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管底部有黑色固体 | 燃烧产物中肯定有C |
| (2) | 取少量(1)所得上层溶液,加入过量的BaCl2溶液 |
| 燃烧产物中肯定有Na2CO3 |
| (3) | 取少量(2)所得上层清液,加入 溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有 |
在步骤(2)中BaCl2溶液为什么要加入至过量?其原因是: 。
【结论】猜想 (填序号)是正确的。
实验室常用的干燥剂“碱石灰”是氧化钙和固体氢氧化钠的混合物,易与空气中的水蒸气和二氧化碳反应而变质。某同学对一瓶久置的碱石灰进行了如下探究:
【猜想与假设】
猜想一:没有变质,只含有氧化钙和氢氧化钠;
猜想二:部分变质;
猜想三:完全变质,含有______________和______________。
则氢氧化钠变质的化学反应方程式是______________________________。
【进行实验】
实验如下图所示:
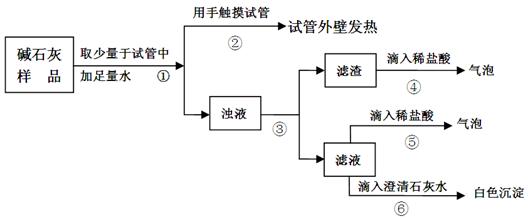 |
【解释与结论】
由操作②的现象判断:猜想三______________(填“成立”或“不成立”);由操作⑤⑥的现象判断滤液中含有_____________,由此判断猜想一不成立,得出结论。
【反思与评价】
实验室中碱石灰应该______________保存。
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究。
探究一:二氧化碳是否与氢氧化钠发生了化学反应 ?
?
同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到 证明二氧化碳与氢氧化钠发生了反应。
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】佳佳认为溶质是Na2CO3
贝贝认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】贝贝为了验证自己的猜想,进行了如下实验,请你补充完整。
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管中,加入足量CaCl2溶液,过滤 ②向滤液滴加适量 |
| 贝贝的猜想成立 |
【实验反思】同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否反生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴边测定混合溶液的pH。请你分析上述方案中,为什么要“当测定pH小于或等于7,”才可证明发生反应了,其原因是
 已知装置B中盛有饱和NaHCO3溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO组成的混合物。整套装置气密性良好,反应所需试剂均足量。
已知装置B中盛有饱和NaHCO3溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO组成的混合物。整套装置气密性良好,反应所需试剂均足量。

