题目内容
19.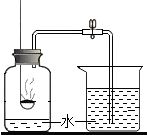 用红磷燃烧测定空气中氧气含量的实验装置如图所示,实验过程中,下列做法会使实验结果产生明显误差的是( )
用红磷燃烧测定空气中氧气含量的实验装置如图所示,实验过程中,下列做法会使实验结果产生明显误差的是( )| A. | 使用过量的红磷 | |
| B. | 把红磷改为蜡烛 | |
| C. | 恢复到实验开始前的温度才进行测量 | |
| D. | 不打开橡胶塞,用放大镜聚焦太阳光点燃红磷 |
分析 本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.
解答 解:
A、使用红磷的量必须足量,才能将密封空气中的氧气全部消耗掉,故选项正确;
B、蜡烛与氧气反应生成的是气体,不可以代替红磷,故选项错误;
C、实验没有等到装置冷却至室温就打开止水夹,由于瓶内气体温度偏高,气压偏大,会导致测量结果小.应恢复到实验开始前的温度才进行测量,故选项正确;
D、用放大镜聚焦太阳光可以达到红磷的着火点,所以不用打开橡胶塞,用放大镜聚焦太阳光点燃红磷,故选项正确.
答案:B
点评 本考点考查的是空气中氧气含量的探究实验,根据实验操作图,回忆实验中现象,由实验中的注意事项,对实验结果进行评价,从而理解该实验的探究目的.对实验结果进行评价,是近几年中考的重点之一,要好好把握.

练习册系列答案
相关题目
10.下列能源属于不可再生能源的是( )
| A. | 煤 | B. | 酒精 | C. | 风能 | D. | 沼气 |
7.某同学就测定Na2CO3和NaCl固体混合物中NaCl的质量分数,分别取mg样品,按下列方案进行试验,合理的是( )
| A. | 与足量稀盐酸充分反应,用排水法收集到 VmL气体 | |
| B. | 与足量BaCl2溶液充分反应,将沉淀过滤、洗涤、干燥,得到m1 g固体 | |
| C. | 与足量AgNO3溶液充分反应,将沉淀过滤、洗涤、干操,得到m2g固体 | |
| D. | 与足量浓盐酸充分反应,逸出的气体用 NaOH固体充分吸收,固体质量增加 m3g |
14.重质碳酸钙粉体产业为我市一大支柱产业,产品远销全国各地.某化学兴趣小组对粉体中碳酸钙含量进行了探究,小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不参与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示.
(1)碳酸钙的相对分子质量为100.
(2)表中m=33.78.
(3)求样品中碳酸钙的质量分数(结果保留两位小数).
| 稀盐酸的总质量(g) | 10.00 | 20.00 | 30.00 | 40.00 | 50.00 | 60.00 | 70.00 |
| 烧杯中物质总质量(g) | 14.66 | 24.22 | m | 43.34 | 52.90 | 62.90 | 72.90 |
(2)表中m=33.78.
(3)求样品中碳酸钙的质量分数(结果保留两位小数).
11.下列食品中富含蛋白质的是( )
| A. | 鲤鱼 | B. | 黄瓜 | C. | 米饭 | D. | 苹果 |
9.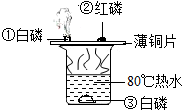 运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
 运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )| A. | ①②现象对比,说明温度达到可燃物的着火点是燃烧条件之一 | |
| B. | ①③现象对比,说明有氧气参与是燃烧条件之一 | |
| C. | 白磷的着火点低于80℃ | |
| D. | 热水只起到加热作用 |
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线. 水者,万物之本.
水者,万物之本.