题目内容
8.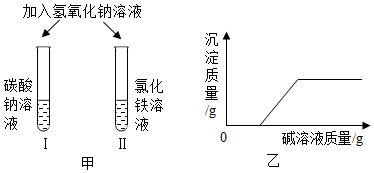 进行如图甲所示的实验,发现试管Ⅰ中产生了沉淀,而试管Ⅱ中无明显现象.
进行如图甲所示的实验,发现试管Ⅰ中产生了沉淀,而试管Ⅱ中无明显现象.【提出问题】向氯化铁溶液中滴加氢氧化钙溶液,为什么没有产生红褐色沉淀?
【作出假设】
假设1:氢氧化钙溶液变质了;
假设2:氢氧化钙的溶解度小,溶液中氢氧根离子的浓度太小;
假设3:氯化铁溶液呈酸性.
请回答下列问题:
(1)验证假设1:如果取氢氧化钙溶液样品与试管中,加入稀盐酸,有气泡产生(请写操作及现象),那么证明氢氧化钙溶液变质了.
(2)为了验证假设3,小明利用pH试纸检验氯化铁溶液,发现氯化铁溶液真的呈酸性.他的操作方法是用玻璃棒蘸取少量待测样品滴在pH试纸上,再与标准比色卡进行对比.那么,在试管Ⅱ中发生了2个反应.
(3)下列物质间反应,最终的沉淀质量和碱溶液质量之间的关系满足如图乙所示图象的是ABC(可多选).
A.HCl和CuCl2的混合液中滴加NaOH B.H2SO4和CuSO4的混合液中滴加KOH
C.HNO3和MgSO4的混合液中滴加NaOH D.HNO3和Na2SO4的混合液中滴加Ba(OH)2.
分析 (1)根据氢氧化钙变质生成了碳酸钙,碳酸钙和盐酸反应会生成二氧化碳气体进行分析;
(2)根据pH试纸测定溶液pH值的正确操作进行分析;
(3)根据图象中的变化趋势可知,开始滴加碱不会生成沉淀,说明碱先与酸反应,然后在于其他物质反应生成沉淀进行分析.
解答 解:(1)氢氧化钙变质生成了碳酸钙,碳酸钙和盐酸反应会生成二氧化碳气体,所以验证假设1:如果取氢氧化钙溶液样品与试管中,加入稀盐酸,有气泡产生,那么证明氢氧化钙溶液变质了;
(2)测定溶液pH值的操作方法是:用玻璃棒蘸取少量待测样品滴在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值,在试管Ⅱ中发生了氯化铁水解生成了盐酸,盐酸和氢氧化钠反应生成了氯化钠和水两个反应;
(3)由图象中的变化趋势可知,开始滴加碱不会生成沉淀,说明碱先与酸反应,然后在于其他物质反应生成沉淀,所以
A.HCl和CuCl2的混合液中滴加NaOH,氢氧化钠先与盐酸反应,再与氯化铜反应,符合图象要求,故A正确;
B.H2SO4和CuSO4的混合液中滴加KOH,氢氧化钾先与硫酸反应,再与硫酸铜反应,符合图象要求,故B正确;
C.HNO3和MgSO4的混合液中滴加NaOH,氢氧化钠会先与硝酸反应,再与硫酸镁反应,符合图象要求,故C正确;
D.HNO3和Na2SO4的混合液中滴加Ba(OH)2,钡离子和硫酸根离子接触就会生成硫酸钡沉淀,故D错误.
故选:ABC.
故答案为:(1)取氢氧化钙溶液样品与试管中,加入稀盐酸,有气泡产生;
(2)用玻璃棒蘸取少量待测样品滴在pH试纸上,3;
(3)ABC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
18.下列有关化合反应和氧化反应的说法中正确的是( )
| A. | 化合反应属于氧化反应 | |
| B. | 某些氧化反应属于化合反应 | |
| C. | 氧化反应是指物质与氧气的反应 | |
| D. | 化合反应是指由多种物质生成新物质的反应 |
16.下列图象能正确反映其对应关系的是( )
| A. | 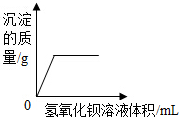 向一定量的硫酸钠和盐酸的混合物溶液中加入氢氧化钡溶液 | |
| B. | 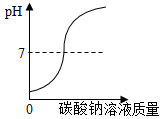 向一定量的盐酸和氯化钙的混合溶液中加入碳酸钠溶液 | |
| C. |  等质量的镁和氧气在点燃条件下充分反应 | |
| D. |  用一定量过氧化氢溶液制取氧气 |
3.下列化学用语中,既可以表示元素符号,也可以表示该元素的一个原子,还可以表示一种物质的是( )
| A. | H | B. | Cl | C. | Cu | D. | H2 |
13.下列物质鉴别的方法错误的是( )
| A. | 区别厨房中的食盐和白糖--分别尝味道 | |
| B. | 区别过氧氢和蒸馏水--加入MnO2,看是否有气泡产生 | |
| C. | 区别硬水与软水--常用肥皂水检验,泡沫少产生浮渣多的是 硬水 | |
| D. | 区别二氧化碳、氧气和空气--分别将带火星的木条伸入瓶中,观察现象 |
20.水是重要的自然资源,与人类生产生活息息相关.但我国淡水资源十分紧缺,所以在生产和生活中应该
( )
( )
| A. | 减少饮水量,以节约用水 | |
| B. | 减少植树造林面积,因为植物生长需要大量的水 | |
| C. | 将洗过菜、洗过衣服的水用来冲洗厕所马桶 | |
| D. | 将工业废水直接排放到江河湖海中,凭借水体自净能力重复使用 |
17. 有一种石灰石样品的成分是CaCO3和SiO2,课外小组同学将100克盐酸分5次加入35克石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2,课外小组同学将100克盐酸分5次加入35克石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
请计算:
(1)第2次加入盐酸后,a为25克
(2)样品中SiO2的质量为15克.
(3)10%的CaCl2溶液可作路面保湿剂.欲将第4次试验后的溶液配成10%的CaCl2溶液,可先向80克盐酸溶液中加入足量的石灰石粉末,完全反应后过滤,这是还需要向滤液中加入多少克水?(假设实验过程中溶液损失忽略不计)
 有一种石灰石样品的成分是CaCO3和SiO2,课外小组同学将100克盐酸分5次加入35克石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2,课外小组同学将100克盐酸分5次加入35克石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)第2次加入盐酸后,a为25克
(2)样品中SiO2的质量为15克.
(3)10%的CaCl2溶液可作路面保湿剂.欲将第4次试验后的溶液配成10%的CaCl2溶液,可先向80克盐酸溶液中加入足量的石灰石粉末,完全反应后过滤,这是还需要向滤液中加入多少克水?(假设实验过程中溶液损失忽略不计)
18.下列关于水的说法不正确的是( )
| A. | 水是生命活动不可缺少的物质 | B. | 肥皂水可以检验硬水和软水 | ||
| C. | 自来水消毒包含化学变化 | D. | 过滤能除去水中所有杂质 |