题目内容
1.科学兴趣小组用以下装置探究炼铁的原理.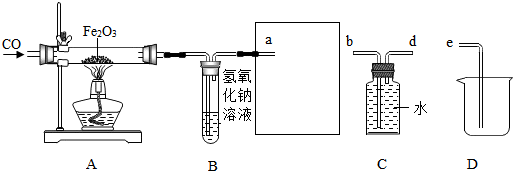
(1)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→d→b→e.(用箭头和接口字母表示)
(2)玻璃管A中发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)根据氢氧化钠溶液能吸收二氧化碳,通过B后的气体是一氧化碳,要收集一氧化碳,应将C中的水排出,将进行分析解答.
(2)根据一氧化碳具有还原性,与氧化铁反应生成铁和二氧化碳,进行分析解答.
解答 解:(1)氢氧化钠溶液能吸收二氧化碳,通过B后的气体是一氧化碳,要收集一氧化碳,应将C中的水排出,长导管是出水管,短导管是进气管,则导管接口的连接顺序为a→d→b→e.
(2)一氧化碳具有还原性,与氧化铁反应生成铁和二氧化碳,玻璃管A中出现的现象为红色固体逐渐变为黑色;反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:(1)d→b→e;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题难度不大,掌握一氧化碳还原氧化铁的反应原理、实验步骤与注意事项等是正确解答本题的关键.

练习册系列答案
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
11.下列生活中的做法,不合理或不能达到目的是( )
| A. | 用肥皂水来区分硬水和软水 | B. | 用活性炭来制作防毒面具 | ||
| C. | 用湿毛巾捂住口鼻逃离火灾现场 | D. | 用一盆水来预防煤气中毒 |
12.现有两组实验小组的同学参与“测定空气中氧气的体积分数”实验.

(1)甲组同学采用课本实验装置(图2),他们先用图1的组合装置在空气中点燃红磷,然后慢慢地将燃烧匙从上到下插入广口瓶中,目的使上、下层空气中的氧气都能得到充分消耗,直到橡皮塞塞紧瓶口,红磷在瓶中继续燃烧直到熄灭,等广口瓶冷却后,打开止水夹.但这样测出的氧气的体积分数明显大于1/5.请分析原因可能向瓶口塞入胶塞过慢由于磷燃烧放热使瓶内气体被赶出一部分
(2)该装置本身在设计上还存在一定的缺陷,也是造成实验误差的原因,请分析其中一种缺陷,说明这种缺陷造成误差的理由燃烧时弹簧夹没有夹紧导致气体受热膨胀而出,最后进入液体多.
(3)乙组同学先查阅资料(如下表),然后对课本上的实验装置进行了图3所示的改进,右端玻璃管上端开口(其它仪器忽略).
①乙组同学红磷换成了白磷的优点是白磷的着火点低,可以较容易的发生燃烧.
②大家用改进的实验装置进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了一段距离,此时他们应该怎样操作之后,才能读取左管页面的刻度待充分反应后.冷却到原来的状况,调整两边的高度使容器左右中的液面保持水平,记录液面刻度.

(1)甲组同学采用课本实验装置(图2),他们先用图1的组合装置在空气中点燃红磷,然后慢慢地将燃烧匙从上到下插入广口瓶中,目的使上、下层空气中的氧气都能得到充分消耗,直到橡皮塞塞紧瓶口,红磷在瓶中继续燃烧直到熄灭,等广口瓶冷却后,打开止水夹.但这样测出的氧气的体积分数明显大于1/5.请分析原因可能向瓶口塞入胶塞过慢由于磷燃烧放热使瓶内气体被赶出一部分
(2)该装置本身在设计上还存在一定的缺陷,也是造成实验误差的原因,请分析其中一种缺陷,说明这种缺陷造成误差的理由燃烧时弹簧夹没有夹紧导致气体受热膨胀而出,最后进入液体多.
(3)乙组同学先查阅资料(如下表),然后对课本上的实验装置进行了图3所示的改进,右端玻璃管上端开口(其它仪器忽略).
| 颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) | |
| 红磷 | 暗红色固体 | 590 | 240 | 2.34 |
| 白磷 | 白色或黄白色固体 | 44.1 | 40 | 1.82 |
②大家用改进的实验装置进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了一段距离,此时他们应该怎样操作之后,才能读取左管页面的刻度待充分反应后.冷却到原来的状况,调整两边的高度使容器左右中的液面保持水平,记录液面刻度.
9.除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )
| 编号 | 物质 | 杂质 | 试剂 | 除杂操作方法 |
| A | CO2 | CO | _ | 点燃 |
| B | CaO | CaCO3 | 水 | 过滤、蒸发 |
| C | NaNO3溶液 | Na2CO3 | 适量CaCl2溶液 | 过滤 |
| D | 铜粉 | 铁粉 | 过量盐酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
16.某校学生用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水.请你帮他完成下列实验探究.
写出C中反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案.
【实验与探究】
(1)甲同学将所有废液倒入乙洁净烧杯中,静置后得到上层清液.
(2)取少量清液加入足量的氯化钡溶液(中性),出现白色沉淀,静置 后向溶液再滴加几滴无色酚酞溶液,溶液变为红色.由此现象说明甲同学所得上层清液中一定含有碳酸钠和氢氧化钠,一定没有氢氧化钙(填物质名称).
| 操作步骤 | 实验现象 | 实验结论 |
| 分别用A,B,C三支试管取样,然后各加入适量碳酸钠溶液 | A中无明显现象 B中产生气泡 C中产生沉淀 | A中的物质是食盐水 B中的物质是稀盐酸 C中的物质是澄清石灰水 |
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案.
【实验与探究】
(1)甲同学将所有废液倒入乙洁净烧杯中,静置后得到上层清液.
(2)取少量清液加入足量的氯化钡溶液(中性),出现白色沉淀,静置 后向溶液再滴加几滴无色酚酞溶液,溶液变为红色.由此现象说明甲同学所得上层清液中一定含有碳酸钠和氢氧化钠,一定没有氢氧化钙(填物质名称).
6.下表中 代表氢原子,
代表氢原子, 代表氧原子,
代表氧原子, 代表碳原子,则下列有关说法不正确的是( )
代表碳原子,则下列有关说法不正确的是( )
 代表氢原子,
代表氢原子, 代表氧原子,
代表氧原子, 代表碳原子,则下列有关说法不正确的是( )
代表碳原子,则下列有关说法不正确的是( )| 物质 | ① | ② | ③ | ④ |
| 分子模型 示意图 |  |  |  |  |
| A. | 上述物质中,①是单质 | |
| B. | 物质②的相对分子质量为18 | |
| C. | 上述物质中,③中氧元素质量分数最大 | |
| D. | 物质③和④组成的元素相同 |
10.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如下:
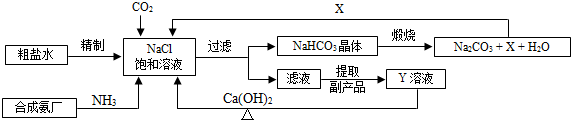
(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为NaOH溶液、BaCl2溶液、Na2CO3溶液或BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸(只写一种).加盐酸的作用是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑、HCl+NaOH═NaCl+H2O.
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由①CO2+NH3+H2O═NH4HCO3和②NaCl+NH4HCO3═NaHCO3↓+NH4Cl两个反应加合而成,则反应类型为复分解反应.
(3)X的化学式为CO2.
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氯化铵,Y的化学式为NH4Cl,写出Y的一种用途氨气.

(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为NaOH溶液、BaCl2溶液、Na2CO3溶液或BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸(只写一种).加盐酸的作用是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑、HCl+NaOH═NaCl+H2O.
| OH- | SO42- | CO32- | |
| Mg2+ | 不 | 溶 | 微 |
| Ca2+ | 微 | 微 | 不 |
| Ba2+ | 溶 | 不 | 不 |
(3)X的化学式为CO2.
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氯化铵,Y的化学式为NH4Cl,写出Y的一种用途氨气.
 “空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题: