题目内容
12. 某同学在实验室发现一瓶标签残缺的硫酸铜溶液.为了测定此溶液的溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数为20%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示.
某同学在实验室发现一瓶标签残缺的硫酸铜溶液.为了测定此溶液的溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数为20%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示.请你仔细分析此关系图,并进行计算.
(1)当滴入氢氧化钠溶液20g时,硫酸铜与氢氧化钠恰好完全反应,此时溶液中的溶质为Na2SO4(填化学式).
(2)计算此硫酸铜溶液中溶质的质量分数(写出解题过程).
分析 (1)由图示可知,当NaOH溶液质量为20g时,沉淀不再生成,说明反应恰好完全;
(2)根据氢氧化钠与硫酸铜反应的化学方程式和氢氧化钠的质量,列出比例式,就可计算出参与反应的CuSO4质量,然后根据质量分数公式计算即可.
解答 解:(1)由图示可知,当NaOH溶液质量为20g时,沉淀不再生成,说明反应恰好完全,此时溶液的溶质为Na2SO4;故答案为:20;Na2SO4
(2)设参与反应的CuSO4质量为x,
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
80 160
20g×20% x
$\frac{80}{20g×20%}=\frac{160}{x}$
x=8g
硫酸铜溶液的溶质的质量分数为:$\frac{8g}{50g}×$100%=16%
答案:
(1)20;Na2SO4;
(2)此硫酸铜溶液中溶质的质量分数为16%.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
20.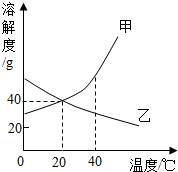 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 20℃时,甲物质的溶解度是40 | |
| B. | 升温可使乙物质的饱和溶液析出固体 | |
| C. | 甲物质的溶解度大于乙物质的溶解度 | |
| D. | 40℃时,将甲、乙两物质饱和溶液分别降温到20℃,二者都变为不饱和溶液 |
4.实验是学习和研究化学的基本方法.下列实验基本操作不正确的是( )
| A. |  读取液体体积 | B. |  闻药品的气味 | ||
| C. |  向试管中滴加液体 | D. |  检查装置的气密性 |
1.下列物质的变化中属于化学变化的是( )
| A. |  冰雪融化 | B. |  水果榨汁 | C. |  分离液态空气 | D. |  葡萄酿酒 |
1.下列各组物质按混合物、纯净物、单质、化合物分类正确的是( )
| A. | 空气、糖水、一氧化碳、铁粉 | B. | 空气、冰水混合物、红磷、二氧化碳 | ||
| C. | 空气、氮气、氢气、澄清石灰水 | D. | 空气、矿泉水、红磷、高锰酸钾 |
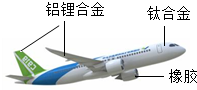 2015年11月,我国首架大型客机C919(如图)正式下线,实现了我国航空领域的新突破.回答下列问题:
2015年11月,我国首架大型客机C919(如图)正式下线,实现了我国航空领域的新突破.回答下列问题:
