题目内容
6.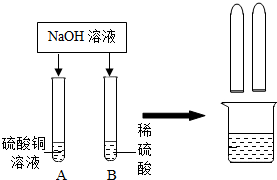 某化学小组在探究碱的化学性质时,做了如图所示的两个实验.
某化学小组在探究碱的化学性质时,做了如图所示的两个实验.(1)写出A试管中发生反应的化学方程式2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(2)实验结束后,同学们将A、B两试管中的废液倒入同一洁净的烧杯,烧杯中出现蓝色沉淀.小组同学将烧杯中的物质进行了过滤,对滤液中成分有如下猜想:
【提出猜想】
甲:滤液中的溶质是Na2SO4 CuSO4
乙:滤液中的溶质是Na2SO4 H2SO4
丙:滤液中的溶质是NaOH、Na2SO4;丁:滤液中的溶质是Na2SO4
【交流讨论】同学们对以上的猜想提出质疑,认为猜想乙不合理,理由是如果滤液中含有稀硫酸,则不可能出现蓝色沉淀.
【设计实验】同学们通过以下的实验对猜想进行验证,请你完成实验报告.
| 实验内容 | 预计现象 | 预计结论 |
| (1)取少量滤液于试管中,观察 | 溶液呈无色 | 猜想甲不成立 |
| (2)继续在上述试管中加入硫酸铜溶液 | 产生蓝色沉淀 | 猜想丙成立 |
分析 (1)氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠;
(2)将A、B两试管中的废液倒入同一洁净的烧杯,烧杯中出现蓝色沉淀,说明甲中硫酸铜过量,乙中氢氧化钠过量;
稀硫酸能和氢氧化铜反应生成硫酸铜和水;
硫酸铜溶液是蓝色的.
解答 解:(1)A试管中发生反应的化学方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
故填:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(2)【提出猜想】
如果氢氧化钠过量,则滤液中的溶质是氢氧化钠和硫酸钠.
故填:NaOH、Na2SO4.
【交流讨论】
猜想乙不合理,理由是如果滤液中含有稀硫酸,则不可能出现蓝色沉淀.
故填:乙;如果滤液中含有稀硫酸,则不可能出现蓝色沉淀.
【设计实验】
(1)取少量滤液于试管中,观察,溶液呈无色,说明溶液在不含有硫酸铜,猜想甲不成立.
故填:甲.
(2)继续在上述试管中加入硫酸铜溶液,产生蓝色沉淀,说明溶液中存在氢氧化钠,猜想丙成立.
故填:硫酸铜溶液;
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.一杯20℃的硝酸钾饱和溶液,欲使其溶质的质量分数变小,下列方法可行的是( )
| A. | 加入一定量的硝酸钾 | B. | 升温到40℃ | ||
| C. | 加入一定量的水 | D. | 恒温蒸发部分水 |
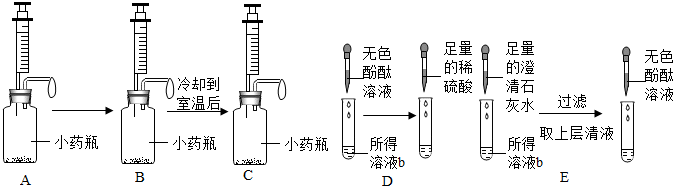
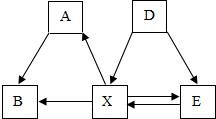 几种常见的物质之间的相互转化关系如图(各字母代表一种物质,各符号表示一个化学反应,部分反应物、生成物及反应条件略去),已知物种物质均有碳、氢、氧中的部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和E可以发生化合反应.
几种常见的物质之间的相互转化关系如图(各字母代表一种物质,各符号表示一个化学反应,部分反应物、生成物及反应条件略去),已知物种物质均有碳、氢、氧中的部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和E可以发生化合反应.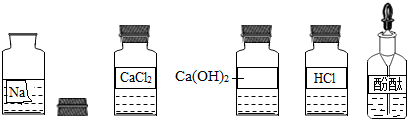
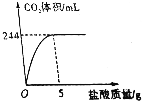 将20g稀盐酸加入到1.25g石灰石样品中反应,生成的CO2体积与加入盐酸质量的关系如图所示(已知本实验条件下CO2的密度为1.8g/L).
将20g稀盐酸加入到1.25g石灰石样品中反应,生成的CO2体积与加入盐酸质量的关系如图所示(已知本实验条件下CO2的密度为1.8g/L).