题目内容
17.在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.例如:2Na+Cl2═2NaCl,反应前后Na、Cl元素的化合价发生了变化,该反应是氧化还原反应.
(1)写出过氧化钙(CaO2)与水反应生成氢氧化钙和氧气的化学方程式2CaO2+2H2O═2Ca(OH)2+O2↑,该反应是否是氧化还原反应是.
(2)硫化氢气体是一种无色有臭鸡蛋气味的有毒气体,其水溶液叫氢硫酸(H2S).氢硫酸跟稀盐酸一样,能与碱发生中和反应,为了防止中毒和污染空气,多余的硫化氢气体可用氢氧化钠溶液吸收,其反应的化学方程式为H2S+2NaOH═Na2S+2H2O.此反应是否是氧化还原反应不是.原因反应前后元素化合价没有改变.
分析 (1)过氧化钙(CaO2)与水反应生成氢氧化钙和氧气的反应的反应物是过氧化钙(CaO2)与水,生成物是氢氧化钙和氧气,反应条件是常温;由于单质的化合价为零,所以氧元素化合价一定变;
(2)根据题意,氢硫酸与盐酸一样能与氢氧化钠溶液发生中和反应,生成硫化钠和水,写出该反应的化学方程式即可.
解答 解:(1)过氧化钙和水反应生成氢氧化钙和氧气,化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑.
氧元素由化合态变成了游离态,化合价发生了变化,故该反应是氧化还原反应;
(2)氢硫酸与盐酸一样能与氢氧化钠溶液发生中和反应,生成硫化钠和水,反应的化学方程式为:H2S+2NaOH═Na2S+2H2O;应前后元素化合价没有改变,故此反应不是氧化还原反应.
故答案为:(1)2 CaO2+2H2O═2Ca(OH)2+O2↑;是;
(2)H2S+2NaOH═Na2S+2H2O;不是;反应前后元素化合价没有改变
点评 本题难度不大,掌握化学方程式的书写等是即可正确解答本题.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
7.下列实验现象中,描述正确的是( )
| A. | 木炭在氧气中剧烈燃烧,生成无色有刺激性气味的气体 | |
| B. | 红磷在氧气中剧烈燃烧,生成大量白色烟雾 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 硫粉在氧气中燃烧,产生蓝紫色火焰 |
8.下列反应中,既属于氧化反应又属于化合反应的是( )
| A. | 汞+氧气$\stackrel{加热}{→}$氧化汞 | B. | 盐酸+氧化钙→氯化钙+水 | ||
| C. | 水 $\stackrel{通电}{→}$氢气+氧气 | D. | 甲烷+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
2.下列有关资源的说法正确的是( )
| A. | 淡水资源占全球总水资源的1%,我们要节约用水 | |
| B. | 空气是一种宝贵的资源,其中稀有气体的体积分数为0.03% | |
| C. | 地壳中含量最多的金属元素是铁元素 | |
| D. | 海水中含量最多的元素是氧元素 |
9.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中的少量CO | 点燃 |
| B | 除去FeSO4溶液中少量CuSO4 | 加入过量的铁粉 |
| C | 鉴别澄清石灰水和NaOH溶液 | 加入稀盐酸 |
| D | 鉴别硬水和软水 | 加入肥皂水 |
| A. | A | B. | B | C. | C | D. | D |
7.以下物质酸性最强的是( )
| A. | 雨水pH=5.6 | B. | 蒸馏水pH=7 | ||
| C. | 厨房清洁剂pH=12.5 | D. | 厕所清洁剂pH=1.6 |
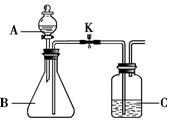 化学小组同学用如图所示装置(夹持仪器已略去)做兴趣实验.
化学小组同学用如图所示装置(夹持仪器已略去)做兴趣实验.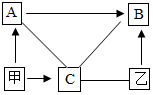 由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲、乙是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.部分反应物、生成物
由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲、乙是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.部分反应物、生成物