题目内容
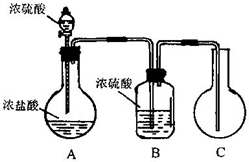
图中是制取一种纯净的气体的装置.试回答:(1)怎样检验图中装置的气密性(C瓶除外)?
(2)用这种方法可以在C瓶中收集到什么气体?
(3)用这种方法制取气体的原理是什么?
(4)B瓶的作用是什么?
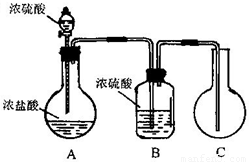
【答案】分析:(1)气密性主要根据内外气压来检测的,瓶内的气压大于外界气压时,插到水中的导气管应该有气泡冒出,如果没有则装置漏气需要重新组装一下,并重新检测.
(2)根据装置的特点和浓硫酸、浓盐酸的性质分析,浓硫酸溶解放时出大量的热且浓硫酸能吸收水,而浓盐酸又具有挥发性.
(3)根据浓硫酸、浓盐酸的性质分析;
(4)根据浓硫酸的吸水性分析.
解答:解:(1)把分液漏斗的开关关上,导气管插到液面以下,用热毛巾裹住锥形瓶,如果有气泡冒出则气密性良好,无气泡冒出则漏气.
(2)浓硫酸溶解时放出大量的热,会使浓盐酸溶液温度升高,气体HCl的溶解度随温度升高而减小,从而释放出来,氯化氢气体中含有水蒸气,通过B装置时水蒸气被浓硫酸吸收,由因为氯化氢气体的密度比空气大,所以用这种方法可以在C瓶中收集到氯化氢气体.
(3)浓硫酸溶解时放出大量的热,会使浓盐酸溶液温度升高,气体HCl的溶解度随温度升高而减小,从而释放出来.
(4)浓硫酸具有吸水性,因此B瓶的作用是除去氯化氢气体中的水蒸气.
故答案为:(1)把分液漏斗的开关关上,导气管插到液面以下,用热毛巾裹住锥形瓶,如果有气泡冒出则气密性良好,无气泡冒出则漏气;
(2)氯化氢气体;
(3)浓硫酸溶解时放出大量的热,会使浓盐酸溶液温度升高,气体HCl的溶解度随温度升高而减小,从而释放出来;
(4)除去氯化氢气体中的水蒸气.
点评:主要考查浓盐酸以及浓硫酸的特性,对于这样的题目,要综合考虑.
(2)根据装置的特点和浓硫酸、浓盐酸的性质分析,浓硫酸溶解放时出大量的热且浓硫酸能吸收水,而浓盐酸又具有挥发性.
(3)根据浓硫酸、浓盐酸的性质分析;
(4)根据浓硫酸的吸水性分析.
解答:解:(1)把分液漏斗的开关关上,导气管插到液面以下,用热毛巾裹住锥形瓶,如果有气泡冒出则气密性良好,无气泡冒出则漏气.
(2)浓硫酸溶解时放出大量的热,会使浓盐酸溶液温度升高,气体HCl的溶解度随温度升高而减小,从而释放出来,氯化氢气体中含有水蒸气,通过B装置时水蒸气被浓硫酸吸收,由因为氯化氢气体的密度比空气大,所以用这种方法可以在C瓶中收集到氯化氢气体.
(3)浓硫酸溶解时放出大量的热,会使浓盐酸溶液温度升高,气体HCl的溶解度随温度升高而减小,从而释放出来.
(4)浓硫酸具有吸水性,因此B瓶的作用是除去氯化氢气体中的水蒸气.
故答案为:(1)把分液漏斗的开关关上,导气管插到液面以下,用热毛巾裹住锥形瓶,如果有气泡冒出则气密性良好,无气泡冒出则漏气;
(2)氯化氢气体;
(3)浓硫酸溶解时放出大量的热,会使浓盐酸溶液温度升高,气体HCl的溶解度随温度升高而减小,从而释放出来;
(4)除去氯化氢气体中的水蒸气.
点评:主要考查浓盐酸以及浓硫酸的特性,对于这样的题目,要综合考虑.

练习册系列答案
相关题目

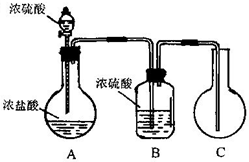 图中是制取一种纯净的气体的装置.试回答:
图中是制取一种纯净的气体的装置.试回答: