题目内容
某黑色粉末A,溶于足量的稀硫酸中呈蓝色透明溶液.现将A进行如下图所示的处理:
(1)判断A、B、C、D、E个各是什么物质?写出其化学式
A ,B ,C ,D ,E .
(2)写出各步反应的化学方程式:
① ;
② ;
③ ;
④ .

(1)判断A、B、C、D、E个各是什么物质?写出其化学式
A
(2)写出各步反应的化学方程式:
①
②
③
④
考点:物质的鉴别、推断,酸的化学性质,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:常见物质的推断题
分析:根据黑色粉末A溶于足量的稀硫酸中呈蓝色透明溶液,所以A是氧化铜,氧化铜和木炭高温会生成二氧化碳和铜,所以B、C是二氧化碳或铜中的一种,而B和炽热的木炭会反应,所以B是二氧化碳,C就是铜,所以D就是一氧化碳,一氧化碳和氧化铜加热会生成铜和二氧化碳,二氧化碳和氢氧化钠会生成碳酸钠和水,所以E是碳酸钠,然后将推出的各种物质代入转化关系中验证即可.
解答:解:(1)黑色粉末A溶于足量的稀硫酸中呈蓝色透明溶液,所以A是氧化铜,氧化铜和木炭高温会生成二氧化碳和铜,所以B、C是二氧化碳或铜中的一种,而B和炽热的木炭会反应,所以B是二氧化碳,C就是铜,所以D就是一氧化碳,一氧化碳和氧化铜加热会生成铜和二氧化碳,二氧化碳和氢氧化钠会生成碳酸钠和水,所以E是碳酸钠,氧化铜和硫酸反应会生成蓝色的硫酸铜和水,氧化铜和木炭高温的条件下会生成铜和二氧化碳,二氧化碳和木炭在高温的条件下会生成一氧化碳,一氧化碳和氧化铜也会生成二氧化碳,二氧化碳和氢氧化钠反应会生成碳酸钠和水,推出的各种物质均满足题意,推导合理,所以A是CuO,B是CO2,C是Cu,D是CO,E是Na2CO3;
(2)反应①是氧化铜和木炭在高温的条件下生成铜和二氧化碳,
化学方程式为:2CuO+C
2Cu+CO2↑,
反应②是二氧化碳和木炭在高温的条件下生成一氧化碳,化学方程式为:CO2+C
2CO,
反应③是一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,化学方程式为:CuO+CO
Cu+CO2,
反应④是氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:CO2+2NaOH=Na2CO3+H2O.
故答案为:(1)CuO,CO2,Cu,CO,Na2CO3;
(2)2CuO+C
2Cu+CO2↑,CO2+C
2CO,CuO+CO
Cu+CO2,CO2+2NaOH=Na2CO3+H2O.
(2)反应①是氧化铜和木炭在高温的条件下生成铜和二氧化碳,
化学方程式为:2CuO+C
| ||
反应②是二氧化碳和木炭在高温的条件下生成一氧化碳,化学方程式为:CO2+C
| ||
反应③是一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,化学方程式为:CuO+CO
| ||
反应④是氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:CO2+2NaOH=Na2CO3+H2O.
故答案为:(1)CuO,CO2,Cu,CO,Na2CO3;
(2)2CuO+C
| ||
| ||
| ||
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
下列没有化学变化发生的是( )
A、 用浓硫酸在纸上写 字 |
B、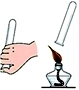 检验氢气的纯度 |
C、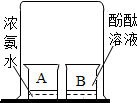 氨分子的运动试验 |
D、 海水晒盐 |
根据下面某反应的微观示意图,结论错误的是( )


| A、该反应为化合反应 |
| B、丙物质属于化合物 |
| C、乙物质中元素的化合价为-2 |
| D、参与反应的甲和乙分子个数比为2:1 |
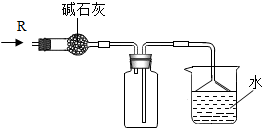 实验室可用如图所示装置干燥(碱石灰是氢氧化钠和生石灰的混合物)、收集气体R,并吸收多余的R,则R可能是( )
实验室可用如图所示装置干燥(碱石灰是氢氧化钠和生石灰的混合物)、收集气体R,并吸收多余的R,则R可能是( )| A、CO2 |
| B、NH3 |
| C、CO |
| D、SO2 |
日常生活中的下列做法不合理的是( )
| A、用纯碱代替洗涤剂洗碗 |
| B、用亚硝酸钠代替食盐调味 |
| C、油锅着火盖锅盖 |
| D、蚊虫叮咬后涂一些含碱性物质的溶液止痒 |
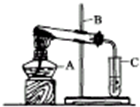 如图是用木炭粉还原氧化铜的装置图.
如图是用木炭粉还原氧化铜的装置图.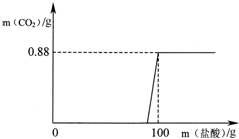 有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体且质量与加入稀盐酸的质量关系如右图所示.试求:样品中碳酸钠的质量是多少g?
有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体且质量与加入稀盐酸的质量关系如右图所示.试求:样品中碳酸钠的质量是多少g?