题目内容
依据氧化铁的化学式Fe2O3,某同学做出下列推断错误的是( )
| A、氧化铁有铁元素和氧元素组成 |
| B、氧化铁中铁元素的化合价是+3 |
| C、氧化铁的相对分子质量为160 |
| D、氧化铁中铁元素的质量分数为68% |
考点:化学式的书写及意义,有关元素化合价的计算,相对分子质量的概念及其计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:A、根据氧化铁化学式Fe2O3进行分析其元素组成;
B、根据在化合物中正负化合价代数和为零,进行解答;
C、根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
D、根据物质中某元素的质量分数的计算方法来分析.
B、根据在化合物中正负化合价代数和为零,进行解答;
C、根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
D、根据物质中某元素的质量分数的计算方法来分析.
解答:解:A、根据氧化铁化学式Fe2O3可知其由铁,氧两种元素组成;故A正确;
B、根据在化合物中正负化合价代数和为零,氧化铁中铁元素的化合价是+3;故B正确;
C、根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得氧化铁的相对分子质量为56×2+16×3=l60;故C正确;
D、根据物质中某元素的质量分数=
×100%,可得氧化铁中铁元素的质量分数=
×100%=70%,故D错误;
故选D.
B、根据在化合物中正负化合价代数和为零,氧化铁中铁元素的化合价是+3;故B正确;
C、根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得氧化铁的相对分子质量为56×2+16×3=l60;故C正确;
D、根据物质中某元素的质量分数=
| 该元素相对原子量×原子个数 |
| 该物质的相对分子量 |
| 56×2 |
| 56×2+16×3 |
故选D.
点评:本题主要考查学生运用化学式进行计算的能力,及根据物质化学式分析其元素组成.

练习册系列答案
相关题目
灭火原理:Na2CO3+2HCl═2NaCl+H2O+R↑中,是推断R的化学式( )
| A、CH4 |
| B、CO2 |
| C、CO |
| D、CCl4 |
下列说法科学的是( )
| A、常用带火星的木条来检验空气中的O2 |
| B、酥脆的饼干在空气中变软是因为空气中含水蒸气 |
| C、氧气的化学性质比较活泼,是可燃物 |
| D、因为氧气与氮气的密度不同,所以工业上分离液态空气法制取氧气 |
下列变化中属于化学变化的是( )
| A、食物腐烂 | B、煤气泄露 |
| C、美酒飘香 | D、铁水铸成铁锅 |
下列关于燃烧现象的描述中正确的是( )
| A、木炭在空气中燃烧后,生成有刺激性气味的气体 |
| B、镁带在空气中燃烧,发出耀眼的白光,生成黑色固体 |
| C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 |
| D、红磷在空气中燃烧,产生大量白雾 |
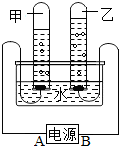 如图是电解水的实验装置,回答下列问题:
如图是电解水的实验装置,回答下列问题: