题目内容
10.请根据图示回答下列问题: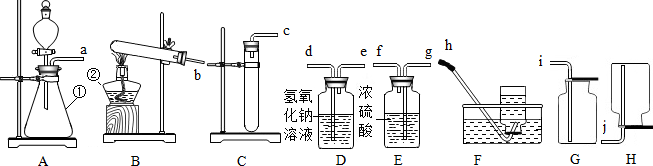
(1)写出图中标号的仪器名称:①锥形瓶,②酒精灯;
(2)实验室用高锰酸钾制取氧气,应选择的气体发生装置是B,产生氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)已知过氧化钠(Na2O2)是一种淡黄色固体,常温下可与水反应生成氢氧化钠和氧气,有关反应化学方程式为2Na2O2+2H2O═4NaOH+O2↑;
(4)某同学用A装置制取CO2,该同学认为他收集到的CO2气体中可能混有HCl气体,他用E装置来检验,应将药品换成硝酸银溶液,他同桌认为不可用D来除去CO2中的HCl气体,原因是因为CO2会与氢氧化钠反应;
(5)实验室制取气体发生装置和收集装置的确定是依据abc(填标号).
a.反应物的状态 b.发生化学反应的条件 c.生成的气体在水中的溶解性和密度.
分析 (1)从仪器和图形和用途去分析解答;
(2)从用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,反应需要加热去分析解答;
(3)从过氧化钠(Na2O2)常温下可与水反应生成氢氧化钠和氧气去分析解答;
(4)从想证明二氧化碳气体中含有HCl气体,HCl气体溶于水形成盐酸,可检验溶液中的氯离子,可加入硝酸银溶液,如果产生氯化银白色沉淀,则证明含有氯化氢气体;由于二氧化碳和氯化氢气体都能和氢氧化钠溶液反应去分析解答;
(5)实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度去分析解答;
解答 解:(1)由仪器和图形和用途可知:①为锥形瓶,②为酒精灯;故答案为:锥形瓶; 酒精灯;
(2)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;由于反应需要加热,所以发生装置应选B;故答案为:B; 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)过氧化钠(Na2O2)常温下可与水反应生成氢氧化钠和氧气,所以其反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑;故答案为:2Na2O2+2H2O═4NaOH+O2↑;
(4)想证明二氧化碳气体中含有HCl气体,HCl气体溶于水形成盐酸,可检验溶液中的氯离子,可加入硝酸银溶液,如果产生氯化银白色沉淀,则证明含有氯化氢气体;由于二氧化碳和氯化氢气体都能和氢氧化钠溶液反应,所以不能用用D来除去CO2中的HCl气体;故答案为:硝酸银溶液; 因为CO2会与氢氧化钠反应;
(5)实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;故答案为:abc.
答案:
(1)①锥形瓶,②酒精灯
(2)B,2KMnO4═K2MnO4+MnO2+O2↑;
(3)2Na2O2+2H2O═4NaOH+O2↑;
(4)硝酸银溶液,因为CO2会与氢氧化钠反应;
(5)abc
点评 实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度.

 阅读快车系列答案
阅读快车系列答案| A. | 黄铜(铜、锌合金)貌似黄金,有人以此冒充黄金行骗,其真伪可用稀盐酸鉴别 | |
| B. | 三种金属原子失去电子能力的大小顺序为:金原子>银原子>铜原子 | |
| C. | 单质铜可以将银从硝酸银溶液中置换出来 | |
| D. | 金、银、铜都属于不活泼金属 |
| A. | 溶质质量 | B. | 溶液质量 | C. | 溶液体积 | D. | 溶质的质量分数 |
| A. | 水变成水蒸气时,只是水分子间的间隔变大了而水分子本身没有变化 | |
| B. | 硫在氧气中燃烧时,硫分子和氧分子都发生变化,结合生成了二氧化硫分子 | |
| C. | 空气里的氧气分子与由高锰酸钾受热分解生成的氧气分子具有不同的化学性质 | |
| D. | 蔗糖放入水中很快就不见了,这是由于蔗糖分子不断运动,脱离了糖块而扩散到水分子中间去的缘故 |
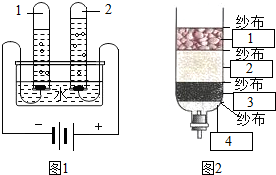 人类的生产和生活都离不开水.
人类的生产和生活都离不开水.