题目内容
20.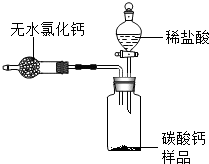 为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2,与稀盐酸不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量,从而计算出样品中碳酸钙的质量分数.为测定生成CO2的质量,他设计了如下实验方案(已知:无水氯化钙是常见的干燥剂):
为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2,与稀盐酸不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量,从而计算出样品中碳酸钙的质量分数.为测定生成CO2的质量,他设计了如下实验方案(已知:无水氯化钙是常见的干燥剂):(1)按图组装好装置,检查装置气密性后,在分液漏斗中加入过量稀盐酸,并在干燥管中加入适量无水氯化钙样品,称得装置和药品的总质量为564.57g;
(2)在广口瓶中加入碳酸钙样品,称得装置和药品的总质量为574.57g;
(3)旋紧橡皮塞,打开分液漏斗旋塞,向广口瓶中滴加稀盐酸,使样品与稀盐酸完全反应;
(4)反应结束后,称得装置及装置内所有物质的总质量为570.57g
请根据上述实验回答下列问题:
(1)该方案测得样品中碳酸钙的质量分数是多少(写出解题过程,计算结果精确到0.1%)?
(2)该实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应,其原因是浓盐酸具有挥发性,会带来测量误差.若实验中不用无水氯化钙干燥,则测得样品中碳酸钙的质量分数与上述实验计算结果相比偏大(选填“偏小”或“不变”或“偏大”).
分析 (1)根据化学方程式和题中参加反应的碳酸钙的质量、生成二氧化碳的质量进行计算;
(2)根据浓盐酸具有挥发性,实验中不用无水氯化钙干燥,会使排出的二氧化碳气体中含有水蒸气,导致结果偏大进行分析.
解答 解:(1)样品的质量为:574.57g-564.57g=10g
生成二氧化碳的质量为:574.57g-570.57g=4g
设参加反应的碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4g
$\frac{100}{x}$=$\frac{44}{4g}$
x=9.09g
所以碳酸钙样品中碳酸钙的质量分数为:$\frac{9.09g}{10g}$×100%=90.9%;
(2)浓盐酸具有挥发性,所以在实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应;实验中不用无水氯化钙干燥,会使排出的二氧化碳气体中含有水蒸气,导致结果偏大.
故答案为:(1)碳酸钙样品中碳酸钙的质量分数为90.9%;
(2)浓盐酸具有挥发性,会带来测量误差,偏大.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
10.下列物质的鉴别方法错误的是( )
| A. | 灼烧法鉴别棉花和羊毛 | |
| B. | 观察颜色鉴别FeCl2溶液和FeCl3溶液 | |
| C. | 肥皂水鉴别硬水和软水 | |
| D. | 白醋鉴别苏打和小苏打 |
11. 2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )
2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )
 2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )
2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )| A. | 农作物的秸杆就地焚烧 | B. | 社会公共场所严禁吸烟 | ||
| C. | 积极开展绿化国土行动 | D. | 工业废水处理达标后排放 |
8.下列关于溶液的说法正确的是( )
| A. | 食用油加入水中,振荡后可形成溶液 | |
| B. | 氢氧化钠固体溶于水时吸收热量,溶液温度降低 | |
| C. | 稀硫酸能够导电,因为溶液中有较多自由移动的离子 | |
| D. | 硝酸钾饱和溶液中加少量氯化钠固体,固体不溶解 |
 2015年12月28日,我市有轨电车(如图)正式通车,关于有轨电车有下列问题,请回答:
2015年12月28日,我市有轨电车(如图)正式通车,关于有轨电车有下列问题,请回答: