题目内容
16. 兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:(1)由pH变化图象可知,在t1时刻,烧杯中存在的阴离子是Cl-和OH-(填写离子符号).
(2)由温度变化图象可知,稀盐酸和氢氧化钠溶液发生的化学反应是放热(选填“放热”或“吸热”)反应.
(3)根据酸和碱反应的特点,可将氢氧化铝制成抗胃酸(主要成分为HCl)药剂,它与另一种抗胃酸药剂碳酸氢钠相比,在建议每次服用剂量下(见表),其药效“强”而且“持久”,其可能原因是:0.25g含Al(OH)3的抗胃酸药剂比0.5g含NaHCO3的抗胃酸药剂能中和更多的HCl,所以药效强于NaHCO3;Al(OH)3和HCl反应速率慢于NaHCO3和HCl,所以药效比服用NaHCO3持久.(提示:NaHCO3+HCl=NaCl+H2O+CO2↑)
| 主要成分 (均占药片质量的95%) | 主要成分的 相对分子质量 | 建议每次 服用剂量/g |
| Al(OH)3 | 78 | 0.25 |
| NaHCO3 | 84 | 0.5 |
分析 (1)根据此时溶液的酸碱度及反应中的物质解答;
(2)根据温度变化图象可知,稀盐酸和氢氧化钠溶液发生放出热量;
(3)根据药品的主要成分与盐酸的反应进行计算分析.
解答 解:(1)由pH变化图象可知,在t1时刻,溶液显碱性,溶液中阴离子有氢氧根离子和氯离子;
(2)由温度变化图象可知,稀盐酸和氢氧化钠溶液发生的反应放出热量;
(3)设0.5g碳酸氢钠消耗盐酸的质量为x,则有
NaHCO3+HCl═NaCl+H2O+CO2↑
84 36.5
0.5g x
$\frac{84}{0.5g}=\frac{36.5}{x}$
x=0.22g
设0.25g氢氧化铝消耗盐酸的质量为y,则有
Al(OH)3+3HCl═AlCl3+3H2O
78 109.5
0.25g y
$\frac{78}{0.25g}=\frac{109.5}{y}$
y=0.35g
通过计算可以看出,0.35gAl(OH)3比0.5gNaHCO3能中和更多的HCl,所以药效强于NaHCO3,
故答案为:(1)Cl-和OH-(2)放热
(3)0.35g含Al(OH)3的抗胃酸药剂比0.5g含NaHCO3的抗胃酸药剂能中和更多的HCl,所以药效强于NaHCO3;Al(OH)3和HCl反应速率慢于NaHCO3和HCl,所以药效比服用NaHCO3持久
点评 本题考查了化学知识在医药方面的应用,完成此题,可以依据酸和碱反应的有关知识进行.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
8.下列鉴别物质的方法中错误的是( )
| A. | 用肥皂水区分硬水和软水 | |
| B. | 观察颜色的方法区分O2和CO2 | |
| C. | 用燃烧的方法区分羊毛和涤纶 | |
| D. | 用pH试纸测定溶液的pH值来区分食盐水和纯碱溶液 |
5.下列图中,体现稀有气体用途的是( )
| A. |  金属切割 金属切割 | B. |  霓虹灯 | C. |  医疗急救 | D. |  灭火 灭火 |
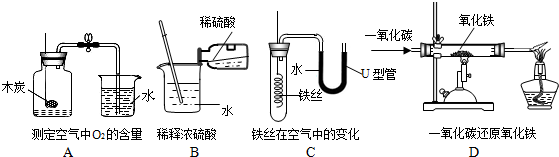
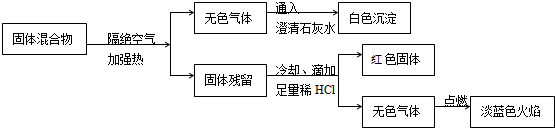
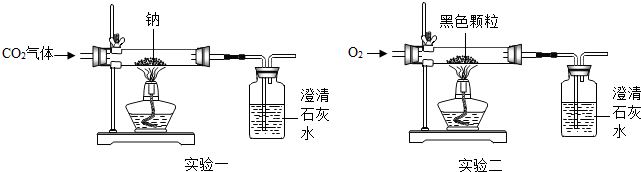
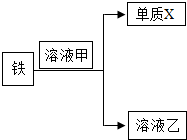 钢铁是生产、生活中使用非常广泛的金属.
钢铁是生产、生活中使用非常广泛的金属.