题目内容
4.蔗糖是储藏在甘蔗、甜菜中的糖,其化学式为C12H22O11.计算:蔗糖中的碳元素的质量分数为$\frac{12×12}{12×12+1×22+16×11}×$100%≈42.1%. (要求写出计算式)
分析 根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:蔗糖中的碳元素的质量分数为$\frac{12×12}{12×12+1×22+16×11}×$100%≈42.1%.
故答案为:$\frac{12×12}{12×12+1×22+16×11}×$100%≈42.1%.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
15.下列关于氧气性质的描述,错误的是( )
| A. | 硫在氧气中燃烧后生成有刺激性气味的气体 | |
| B. | 氧气在低温、高压时能变成淡蓝色液体或固体 | |
| C. | 氧气极易溶于水 | |
| D. | 氧气是一种化学性质比较活泼的气体 |
19.下列化学实验操作正确的是( )
| A. | 胶头滴管未清洗吸取和滴加不同液体 | |
| B. | 实验结束后,剩余药品都应放回原试剂瓶 | |
| C. | 给试管里的药品加热时,应先进行预热 | |
| D. | 鼻孔直接凑到容器口闻药品的气味 |
9.车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.
(1)写出乙醇在氧气中完全燃烧的化学方程式C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种在氧气不充足条件下不充分燃烧的产物w.
现测得反应前后各物质的质量如下:
根据质量守恒定律,得出表中x的值为14;
(3)为了使乙醇汽油燃烧过程中少产生w,应采取的措施是加大空气的进入量.
(1)写出乙醇在氧气中完全燃烧的化学方程式C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种在氧气不充足条件下不充分燃烧的产物w.
现测得反应前后各物质的质量如下:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水蒸气 | w |
| 反应前质量/g | 23 | 40 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 22 | 27 | x |
(3)为了使乙醇汽油燃烧过程中少产生w,应采取的措施是加大空气的进入量.
11.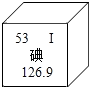 日本“3•11”大地震及其引发的海啸造成日本福岛核电站受损而释放出大量人工放射性元素碘-131(131表示原子的质量数).如图是元素周期表中碘元素的相关信息,下列说法不正确的是( )
日本“3•11”大地震及其引发的海啸造成日本福岛核电站受损而释放出大量人工放射性元素碘-131(131表示原子的质量数).如图是元素周期表中碘元素的相关信息,下列说法不正确的是( )
 日本“3•11”大地震及其引发的海啸造成日本福岛核电站受损而释放出大量人工放射性元素碘-131(131表示原子的质量数).如图是元素周期表中碘元素的相关信息,下列说法不正确的是( )
日本“3•11”大地震及其引发的海啸造成日本福岛核电站受损而释放出大量人工放射性元素碘-131(131表示原子的质量数).如图是元素周期表中碘元素的相关信息,下列说法不正确的是( )| A. | 碘元素的元素符号是I | |
| B. | 碘元素的相对原子质量为126.9 g | |
| C. | 一个碘-131原子的原子核内有78个中子 | |
| D. | 碘元素属于非金属元素 |
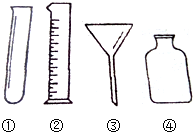 下列仪器室化学实验常用的仪器.
下列仪器室化学实验常用的仪器.