题目内容
8.某石灰厂需要测定产品生石灰中杂质(杂质只含CaCO3)的质量分数.小刚进行了如图实验.请计算: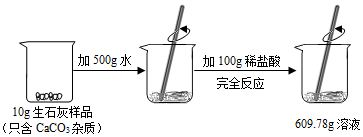
(1)生成CO2气体的质量(假设气体全部逸出,不考虑水蒸气的影响);
(2)样品中CaCO3的质量分数.
分析 根据反应前后的质量差可以求出生成二氧化碳的质量,根据二氧化碳的质量可以求出碳酸钙的质量.
解答 解:(1)反应前后的质量差即是生成的二氧化碳的质量,生成的二氧化碳的质量为:10g+500g+100g-609.78g=0.22g,
(2)设样品中CaCO3的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 0.22g
$\frac{100}{44}=\frac{x}{0.22g}$
x=0.5g
样品中CaCO3的质量分数为:$\frac{0.5g}{10g}$×100%=5%.
答:(1)生成CO2气体的质量为0.22g;
(2)样品中CaCO3的质量分数为5%.
点评 解答本题关键是要能够通过反应前后的质量差,求出生成的二氧化碳的质量,其它计算就迎刃而解了.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.在过氧化氢制氧气的化学变化的过程中,最小的粒子是( )
| A. | H2O2 | B. | H2O | C. | O2 | D. | H和O |
16.下列实验操作正确的是( )
| A. | 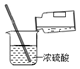 稀释浓硫酸 | B. | 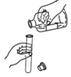 倾倒液体 | C. | 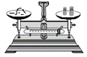 称量固体 | D. | 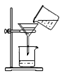 过滤 |
3.一氧化碳与氢气在一定条件下发生反应的化学方程式是2CO+4H2 $\frac{\underline{\;一定条件\;}}{\;}$ X+H2O.下列分析正确的是( )
| A. | X中只含C、H元素 | B. | X与CO的相对分子质量之差为16 | ||
| C. | 该反应的基本类型是置换反应 | D. | X中C、H元素质量比为4:1 |
20.下列化学方程式书写正确的是( )
| A. | 木炭和氧化铜反应:C+2CuO=2Cu+CO2↑ | |
| B. | 镁在空气中燃烧:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | |
| C. | 过氧化氢分解:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑ | |
| D. | 硝酸银溶液和氯化钠溶液反应:AgNO3+NaCl=NaNO3+AgCl |
17.下列变化属于化学变化的是( )
| A. | 香水挥发 | B. | 食物腐败 | C. | 玻璃破碎 | D. | 冰雪熔化 |