题目内容
在一个密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
| 物质 | A | B | C | D |
| 反应前质量 (g) | 9 | 2 | 22 | 1 |
| 反应后质量(g) | x | 2 | 6 | 21 |
(1)X=______;
(2)该反应的反应类型是哪一种?
(3)若A、C两种物质的相对分子质量之比是1:2,请写出用A、B、C、D表示的该反应的化学方程式.
解:(1)由表中数据分析可知,反应前后,B的质量不变,且B物质的化学性质在反应前后未发生变化,故B可能作该反应的催化剂,也可能没发生化学反应;C的质量减少了16g,故C是反应物,参加反应的C的质量为16g;同理可以确定D是生成物,生成的D的质量为20g;由质量守恒定律,A应是反应物,且参加反应的A的质量为20g-16g=4g,故x的数值为9g-4g=5g.
(2)该反应的反应物为A和C,生成物是D,符合“多变一”的特征,属于化合反应.
(3)根据题意,A、C两种物质的相对分子质量之比是1:2,设A的相对分子质量为M,则C的相对分子质量为2M,则
aA+bC=D
Ma 2Mb
4g 16g
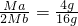
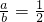
故反应的化学方程式为A+2C=D.
故答案为:(1)X=5;(2)化合反应;(3)A+2C=D.
分析:本题可分析先B、C、D三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定A是反应物还是生成物,进而可以确定反应类型;由A、C两种物质的相对分子质量之比是1:2,可以计算出A、B两物质的化学计量数之比,进而用A、B、C、D表示的该反应的化学方程式.
点评:本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.
(2)该反应的反应物为A和C,生成物是D,符合“多变一”的特征,属于化合反应.
(3)根据题意,A、C两种物质的相对分子质量之比是1:2,设A的相对分子质量为M,则C的相对分子质量为2M,则
aA+bC=D
Ma 2Mb
4g 16g
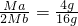
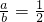
故反应的化学方程式为A+2C=D.
故答案为:(1)X=5;(2)化合反应;(3)A+2C=D.
分析:本题可分析先B、C、D三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定A是反应物还是生成物,进而可以确定反应类型;由A、C两种物质的相对分子质量之比是1:2,可以计算出A、B两物质的化学计量数之比,进而用A、B、C、D表示的该反应的化学方程式.
点评:本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
24、在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的认识不正确的是( )
|

