题目内容
4.某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案.有关该实验流程分析正确的是( )
| A. | X是锌 | |
| B. | Y是稀硫酸 | |
| C. | 滤液1中含有Fe2+和Cu2+ | |
| D. | 操作a和操作b中使用的玻璃棒的作用一样 |
分析 想从含有FeSO4、CuSO4的废液中回收金属铜和硫酸亚铁晶体,应加入过量的金属X是铁,铁与硫酸铜反应生成了硫酸亚铁和铜,过滤得到铜和铁的混合金属,在几十辆的稀硫酸将铁除去,将滤液12蒸发得到硫酸冶铁晶体.据此分析回答有关的问题.
解答 解:由题意可知,想从含有FeSO4、CuSO4的废液中回收金属铜和硫酸亚铁晶体,应加入过量的金属X是铁,铁与硫酸铜反应生成了硫酸亚铁和铜,过滤得到铜和铁的混合金属,在几十辆的稀硫酸将铁除去,将滤液12蒸发得到硫酸冶铁晶体.所以:
A、由上述分析可住,X是铁,故A错误;
B、Y是稀硫酸,故B正确;
C、由于加入的铁粉是过量的,滤液1中只含有Fe2+,故C错误;
D、由实验的过程可知,操作a是过滤,操作b是蒸发,使用玻璃棒的作用不一样,故D错误.
故选B.
点评 本题主要考查了金属活动性顺序表的应用,难度不大,熟记金属活动性顺表、理解其应用是解答本题的关键,另外还要熟知除杂的原则及化学方程式的书写.

练习册系列答案
相关题目
3.下列关于化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5的读法,错误的是( )
| A. | 磷和氧气在点燃的条件下反应生成五氧化二磷 | |
| B. | 在点燃的条件下,每4体积的磷和5体积的氧气完全反应,生成五氧化二磷 | |
| C. | 在点燃的条件下,每4个磷原子和5个氧气分子结合生成2个五氧化二磷分子 | |
| D. | 在点燃的条件下,每124份质量的磷和160份质量的氧气完全反应,生成284份质量的五氧化二磷 |
1. 如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
 如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | 通过升温可以将甲的不饱和溶液变为饱和溶液 | |
| B. | 20℃时分别将甲、乙溶液蒸发相等质量的水,析出甲、乙的质量相等 | |
| C. | 10℃时,10g水中分别溶解甲、乙达到饱和溶液,溶解较多的物质是乙 | |
| D. | 把100g溶质质量分数为10%的乙溶液从30℃降温到10℃,其质量分数仍为10% |
9.如图所示的实验操作,正确的是( )
| A. | 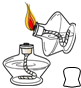 点燃酒精灯 | B. | 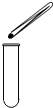 取锌粒 | C. | 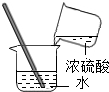 稀释浓硫酸 | D. | 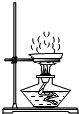 蒸发 |
13.水是成产生活中不可缺少的物质.下列关于水的说法中正确的是( )
| A. | 明矾溶液可用区分硬水和软水 | |
| B. | 长期饮用蒸馏水有利于人体健康 | |
| C. | 水与过氧化氢的组成元素相同,均可用于制备氧气 | |
| D. | 活性炭可以吸附可溶性的颜色、异味、也可以滤去难溶物,活性炭过滤的水一定是纯净物 |


