题目内容
(1)已知常温下铁能与氯化铁反应生成氯化亚铁,铜也能与氯化铁溶液反应生成氯化亚铁和氯化铜.写出这两个反应的方程式 .
现将铁粉和铜粉加入到一定量氯化铁溶液中,反应后固体成分的分析中,则下列情况中不可能出 (填序号)
A.有铁有铜 B.有铁无铜 C.无铁无铜 D.无铁有铜
(2)小明在实验室中找到一根铝丝,准备做铝和硫酸铜溶液的反应,验证金属铝和金属铜的活泼性.老师告诉小明在硫酸铜溶液中有一定量的硫酸,小明把足量铝条插入到这样的硫酸铜溶液中后,一段时间后才看到有红色固体析出,并看到有气泡生成.已知金属氧化物可以和酸反应生成金属化合物和水.请写出整个过程中发生反应的化学方程式 .
(3)地球上水资源非常宝贵,爱护水资源主要从(填代号) 方面采取措施.
A.南水北调 B.节约用水 C.防止水体污染 D.工、农业不用水.
现将铁粉和铜粉加入到一定量氯化铁溶液中,反应后固体成分的分析中,则下列情况中不可能出
A.有铁有铜 B.有铁无铜 C.无铁无铜 D.无铁有铜
(2)小明在实验室中找到一根铝丝,准备做铝和硫酸铜溶液的反应,验证金属铝和金属铜的活泼性.老师告诉小明在硫酸铜溶液中有一定量的硫酸,小明把足量铝条插入到这样的硫酸铜溶液中后,一段时间后才看到有红色固体析出,并看到有气泡生成.已知金属氧化物可以和酸反应生成金属化合物和水.请写出整个过程中发生反应的化学方程式
(3)地球上水资源非常宝贵,爱护水资源主要从(填代号)
A.南水北调 B.节约用水 C.防止水体污染 D.工、农业不用水.
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式,保护水资源和节约用水
专题:金属与金属材料
分析:(1)根据反应物和生成物依据化学方程式书写的步骤写出反应的化学方程式即可;
在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,向盛有FeCl3溶液的烧杯内加入铁粉和铜粉,铁能与氯化铁反应生成氯化亚铁,铜能与氯化铁反应生成氯化亚铁和氯化铜,铁能与生成的氯化铜反应生成氯化亚铁和铜.溶液中离子反应,应遵循氧化性、还原性强弱顺序反应;
(2)根据铝的活动性比铜强,将铝丝插入到硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜解答;
(3)根据教材中所学习的有关水资源状况的知识,以及保护水资源和节约用水的知识可以作答.
在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,向盛有FeCl3溶液的烧杯内加入铁粉和铜粉,铁能与氯化铁反应生成氯化亚铁,铜能与氯化铁反应生成氯化亚铁和氯化铜,铁能与生成的氯化铜反应生成氯化亚铁和铜.溶液中离子反应,应遵循氧化性、还原性强弱顺序反应;
(2)根据铝的活动性比铜强,将铝丝插入到硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜解答;
(3)根据教材中所学习的有关水资源状况的知识,以及保护水资源和节约用水的知识可以作答.
解答:解:
(1)铁能与氯化铁反应生成氯化亚铁反应的方程式为:2FeCl3+Fe═3FeCl2;氯化铁能与铜反应生成氯化铜和氯化亚铁,反应的方程式为:2FeCl3+Cu═2FeCl2+CuCl2;
向盛有FeCl3溶液的烧杯内加入铁粉和铜粉,铁能与氯化铁反应生成氯化亚铁,铜能与氯化铁反应生成氯化亚铁和氯化铜,过量铁能与生成的氯化铜反应生成氯化亚铁和铜;
A、加入的铁粉和铜粉足量,Fe3+、Cu2+,不会有剩余,该结果可能出现,故错误;
B、加入铁和铜的混合物,铁首先与氯化铁反应,溶液中无Cu,则一定没有Fe3+,该结果不可能出现,故B正确;
C、加入铁和铜的混合物,烧杯中铁、铜都无,可能是全部将铁离子反应完毕,只反应了部分铜离子,该结果可能出现,故错误;
D、加入铁和铜的混合物,铁首先与氯化铁反应,可能铁全部反应而铜有剩余,该结果可能出现,故错误.
(2)铝的化学性质比较活泼,能被氧气氧化成一层氧化物薄膜,该氧化物是氧化铝,氧化铝和稀硫酸反应能生成硫酸铝和水,反应的化学方程式为:3H2SO4+Al2O3=Al2(SO4)3+3H2O.
铝的活动性比铜强,将铝丝插入到硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜,可观察到铝丝表面出现红色固体,溶液由蓝色逐渐变为无色,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu.
(3)爱护水资源主要从节约用水和防止水体污染两方面采取措施.故填:B、C.
答案:
(1)2FeCl3+Fe═3FeCl2;2FeCl3+Cu═2FeCl2+CuCl2; B
(2)3H2SO4+Al2O3=Al2(SO4)3+3H2O;2Al+3CuSO4=Al2(SO4)3+3Cu
(3)BC
(1)铁能与氯化铁反应生成氯化亚铁反应的方程式为:2FeCl3+Fe═3FeCl2;氯化铁能与铜反应生成氯化铜和氯化亚铁,反应的方程式为:2FeCl3+Cu═2FeCl2+CuCl2;
向盛有FeCl3溶液的烧杯内加入铁粉和铜粉,铁能与氯化铁反应生成氯化亚铁,铜能与氯化铁反应生成氯化亚铁和氯化铜,过量铁能与生成的氯化铜反应生成氯化亚铁和铜;
A、加入的铁粉和铜粉足量,Fe3+、Cu2+,不会有剩余,该结果可能出现,故错误;
B、加入铁和铜的混合物,铁首先与氯化铁反应,溶液中无Cu,则一定没有Fe3+,该结果不可能出现,故B正确;
C、加入铁和铜的混合物,烧杯中铁、铜都无,可能是全部将铁离子反应完毕,只反应了部分铜离子,该结果可能出现,故错误;
D、加入铁和铜的混合物,铁首先与氯化铁反应,可能铁全部反应而铜有剩余,该结果可能出现,故错误.
(2)铝的化学性质比较活泼,能被氧气氧化成一层氧化物薄膜,该氧化物是氧化铝,氧化铝和稀硫酸反应能生成硫酸铝和水,反应的化学方程式为:3H2SO4+Al2O3=Al2(SO4)3+3H2O.
铝的活动性比铜强,将铝丝插入到硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜,可观察到铝丝表面出现红色固体,溶液由蓝色逐渐变为无色,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu.
(3)爱护水资源主要从节约用水和防止水体污染两方面采取措施.故填:B、C.
答案:
(1)2FeCl3+Fe═3FeCl2;2FeCl3+Cu═2FeCl2+CuCl2; B
(2)3H2SO4+Al2O3=Al2(SO4)3+3H2O;2Al+3CuSO4=Al2(SO4)3+3Cu
(3)BC
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号及化学方程式的书写,考查全面,注重基础.本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
如图为某一反应的微观示意图,下列说法错误的是( )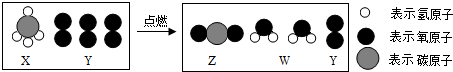

| A、X是化合物,Y是单质 | ||||
| B、X物质中碳元素的质量分数为75.0% | ||||
C、该反应的化学方程式式:CH4+O2
| ||||
| D、点燃X前,要先检验其纯度 |
生活中的许多物质外观非常相似,需要通过一定的方法去鉴别.下列有关物质的鉴别方法不能达到目的是( )
| A、用肥皂水鉴别硬水和软水 |
| B、用燃烧的方法鉴别真假毛线 |
| C、用水鉴别氯化钾和碳铵 |
| D、用紫色石蕊试液鉴别食盐水和白醋 |
下列各组物质(最后一种物质是过量的),加足量的水混合后,能得到无色溶液,无沉淀产生,又无气体生成的是( )
| A、Ba(OH)2、MgCl2、HCl |
| B、CuO、HCl、AgNO3 |
| C、FeCl3、KOH、HCl |
| D、CaO、Na2CO3、HNO3 |
化学基本概念是学好化学的基础,对下列有关概念的认识正确的是( )
| A、原子是最小的微粒,不可再分 |
| B、化合反应都是氧化反应 |
| C、只有燃烧才能产生放热现象 |
| D、保持氧气化学性质的最小粒子是氧分子 |
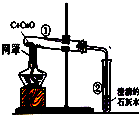 用木炭还原氧化铜的实验如图.
用木炭还原氧化铜的实验如图.