题目内容
16.如图是实验室制取气体时常见的装置(其中F、I为干燥装置),根据装置回答下列问题: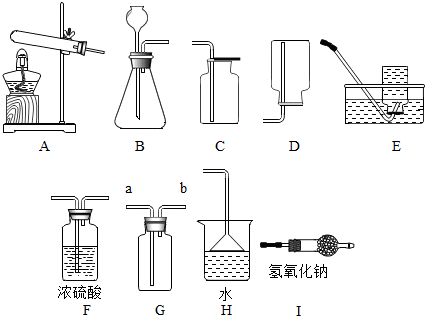
(1)用B装置制取的某气体可使带火星的木条复燃,请写出用B装置制取该气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)选择气体发生装置A或B时应考虑的因素有反应物的状态和反应的条件;若用G装置收集CO2气体,气体应从a(填“a”或“b”)通入.
(3)常温下,氨气(NH3)是一种有刺激性气味的气体,极易溶于水,密度比空气小,溶液呈碱性.实验室制取氨气的原理是NH4C1(固)与Ca(OH)2(固)混合共热.现要制取和收集干燥的氨气并处理尾气,防止污染空气,所选择的装置连接顺序依次是A→I→G→H(填装置序号).
分析 (1)根据装置特点和气体特性来确定制取气体的方法;
(2)要根据制取气体的反应原理来选择气体发生装置,根据二氧化碳的密度来确定收集方法;
(3)氨气能和浓硫酸反应,不能用浓硫酸干燥氨气,氨气不能和氢氧化钠反应,可以用氢氧化钠干燥氨气.
解答 解:(1)B装置适用于固液常温下制取氧气,是用二氧化锰作催化剂分解过氧化氢来制取氧气;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)实验室选择气体发生装置时应考虑的因素是反应物的状态,反应条件等.固体加热制取气体选择A装置;固液常温下制取气体选择装置B来制取;收集密度比空气大的气体,应从长管进气,二氧化碳的密度比空气大;故填:反应物的状态和反应的条件;a;
(3)固体加热来制取氨气则用装置A来制取氨气,要制得干燥的氨气,需要用氢氧化钠固体干燥氨气,不能用浓硫酸干燥,因为浓硫酸会和氨气发生反应,用G来收集,最后用水来吸收多余的氨气.故填:A→I→G→H.
点评 本题综合考查了学生的基本实验能力,涉及仪器的用途、化学方程式的书写、装置选择、实验基本操作等知识,只有综合理解化学知识才能够正确的解答.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
11.下列除去杂质的试剂和方法可行的是( )
| 选项 | 物质(括号内为杂质) | 除杂试剂和方法 |
| A | CO2(CO) | 通过足量澄清石灰水 |
| B | N2(O2) | 通过灼热的氧化铜 |
| C | Mg(NO3)2溶液(AgNO3) | 加入过量铁粉,过滤 |
| D | NaCl溶液(Na2SO4) | 加入适量BaCl2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
8.下列四幅坐标图分别所表示的意义不正确的是( )
| A. | 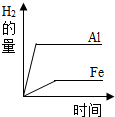 分别将等质量的铝和铁放入足量的盐酸中,放出H2的量的变化 | |
| B. | 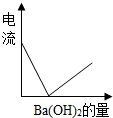 做溶液导电性实验:向一定量的硫酸铜溶液中逐滴滴入Ba(OH)2溶液至过量,则通过溶液的电流变化 | |
| C. | 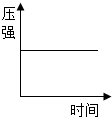 将足量的硫点燃后放入盛氧气的集气瓶中燃烧,并塞紧瓶塞,瓶内压强的变化 | |
| D. |  加热一定量氯酸钾和二氧化锰的固体混合物,二氧化锰的质量分数随加热时间的变化 |
5.小明同学分别取20gNaOH固体A、B、C,采用不同方法保存.几天后,A未变质、B部分变质、C全部变质,他将三份固体分别配成溶液并滴入20%的稀硫酸直到正好反应.下列说法正确的是( )
| A. | 几天后,三份固体的质量为:A=B=C | |
| B. | 为控制正好反应,A能用酚酞试液指示,B、C可滴加稀硫酸直到正好不冒气泡 | |
| C. | 正好反应时,消耗稀硫酸的质量由大到小的顺序为:A>B>C | |
| D. | 正好反应时,生成硫酸钠的质量都相等,均为35.5g |
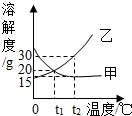 (1)如图是甲、乙两物质的溶解度曲线,试回答:
(1)如图是甲、乙两物质的溶解度曲线,试回答: