题目内容
20.用化学符号或名称填空.(1)碳元素C;
(2)H+氢离子;
(3)NO3-硝酸根离子;
(4)氯化锌ZnCl2;
(5)3个氮分子3N2.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)元素可用元素符号表示,碳元素的元素符号为:C;
(2)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故H+表示:氢离子;
(3)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故NO3-表示硝酸根离子;
(4)氯化锌是由显+2价的锌元素和显-1价的氯元素组成,根据化合价原则,其化学式为:ZnCl2;
(5)由分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,3个氮分子可表示为:3N2;
故答案为:(1)C;(2)氢离子;(3)硝酸根离子;(4)ZnCl2;(5)3N2;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
10.下列变化中,属于物理变化的是( )
| A. | 爆竹爆炸 | B. | 食醋除水垢 | C. | 石油分馏 | D. | 葡萄酿酒 |
11.下列变化中,都属于物理变化的一组是( )
| A. | 铁器生锈 水果腐烂 | |
| B. | 水的蒸发 水的电解 | |
| C. | 活性炭除去冰箱中的异味 石蜡燃烧 | |
| D. | 氢氧化钠固体潮解 汽油挥发 |
8.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
15.下列物质属于混合物的是( )
| A. | 矿泉水 | B. | 高锰酸钾 | C. | CuSO4•5H2O | D. | 液氧 |
12.以下物质因为具有良好的吸水性,常用作气体的干燥剂,其中吸水过程中一定发生了化学变化的是( )
| A. | 浓硫酸 | B. | 生石灰 | C. | 烧碱固体 | D. | 氯化钙固体 |

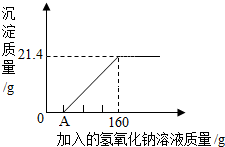 某化工厂的废水中只含有稀盐酸和氯化铁,小敏采集了该废水样品95.4g,并向其中滴加20%的氢氧化钠溶液至恰好完全反应,测得所加入的氢氧化钠溶液质量与反应生成的沉淀质量关系如图所示,已知上述反应后所得溶液在常温下为不饱和溶液,求该溶液中溶质的质量分数.
某化工厂的废水中只含有稀盐酸和氯化铁,小敏采集了该废水样品95.4g,并向其中滴加20%的氢氧化钠溶液至恰好完全反应,测得所加入的氢氧化钠溶液质量与反应生成的沉淀质量关系如图所示,已知上述反应后所得溶液在常温下为不饱和溶液,求该溶液中溶质的质量分数.