题目内容
4.现摘自某制药有限公司生产的“钙尔奇D600片剂”的部分文字说明如下:①本品“每片含主要成分碳酸钙1.5g(相当于钙600mg),成人每天服用1片”.你知道“1.5g碳酸钙与600mg钙”的计量关系是如何得出来的吗?1.5g×$\frac{40}{100}$×100%=0.6g=600mg.
②根据你理解的上述计量关系,则该公司的另一产品“钙尔奇D300片剂”中,每片含主要成分碳酸钙0.75克;若改服此产品,则成人每天需服用2片.
分析 根据碳酸钙的质量、钙元素的质量分数可以计算一定质量的碳酸钙中含有钙元素的质量.
解答 解:(1)1.5g碳酸钙中,钙元素的质量为:1.5g×$\frac{40}{100}$×100%=0.6g=600mg,所以1.5g碳酸钙中含有600mg钙元素;
(2)“D300片剂”中,设每片含主要成分碳酸钙的质量为X,
则有:X×$\frac{40}{100}$×100%=300mg,
X=750mg=0.75g,
若改服此产品.则成人每天需服用2片.
故答案为:(1)1.5g×$\frac{40}{100}$×100%=0.6g=600mg;(2)0.75;2.
点评 本题是一道生化结合题,解决本题的关健是明确元素与人体健康的关系,元素的吸收途径以及根据化学式的计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
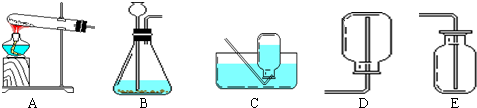
13.如图为初中化学常见气体的发生、收集装置.有关这些装置的说法不正确的是( )
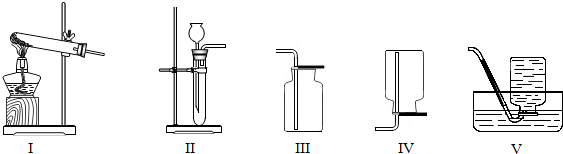

| A. | 装置Ⅰ可作为加热固体制取气体的发生装置 | |
| B. | 装置Ⅱ可用于制取二氧化碳气体,也可以用于制取氧气 | |
| C. | 装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应色无毒气体 | |
| D. | 装置Ⅳ、Ⅴ都可用于实验室收集氧气 |
9.某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答:
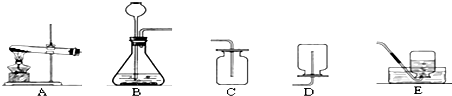
(1)若用加热高锰酸钾来制取并收集较干燥的氧气,应选用的装置组合是AC(填装置序号),在加入药品之前,应进行的操作是检查装置的气密性.
(2)若用E装置收集氧气,水槽中出现紫红色,最可能的原因是试管口没放棉花团;
(3)某同学观察到发生装置内有大量气泡时,开始用C装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都末见木条复燃.其原因是装置气密性不好.
(4)用C装置收集气体时,在给药品加热时候开始收集气体.
(5)瑞利和拉姆塞两位科学家在利用氨氧化原理进行实验时,所需氨气的制取反应原理如下:2NH4Cl(固体)+Ca(OH)2(固)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
已知空气、氨气在标准状况下的密度和溶解性如表:
根据上述信息,请你帮助两位科学家选择实验室制取氨气的发生装置是A,收集氨气的装置是D.(填上表装置图的编号)

(1)若用加热高锰酸钾来制取并收集较干燥的氧气,应选用的装置组合是AC(填装置序号),在加入药品之前,应进行的操作是检查装置的气密性.
(2)若用E装置收集氧气,水槽中出现紫红色,最可能的原因是试管口没放棉花团;
(3)某同学观察到发生装置内有大量气泡时,开始用C装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都末见木条复燃.其原因是装置气密性不好.
(4)用C装置收集气体时,在给药品加热时候开始收集气体.
(5)瑞利和拉姆塞两位科学家在利用氨氧化原理进行实验时,所需氨气的制取反应原理如下:2NH4Cl(固体)+Ca(OH)2(固)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
已知空气、氨气在标准状况下的密度和溶解性如表:
| 物质 | 空气 | 氨气 |
| 密度/(g/L) | 1.293 | 0.771 |
| 溶解性 | / | 极易溶于水 |
13.下列说正确的是( )
| A. | 分子里一定有原子 | |
| B. | 在物理变化中,分子的组成和结构发生了改变 | |
| C. | 分子大,原子小 | |
| D. | 决定原子质量大小的主要是质子和电子 |

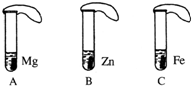 一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图).
一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图).