题目内容
1.A-K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转换关系如图所示.
(1)D,F的化学式:DCu(OH)2,FCO2;
(2)①的基本反应类型是复分解反应;
(3)反应②的化学方程式是Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)气体E的用途是冶炼金属.
分析 根据A-K为中学常见的物质,H是一种建筑材料的主要成分,H是白色沉淀,所以H是碳酸钙,气体F和溶液G反应会生成碳酸钙,所以F是二氧化碳,G是氢氧化钙,固体I和硝酸银反应会生成蓝色溶液和银白色固体K,所以I是铜,J是硝酸铜,K是银,A为黑色粉末,A和气体E加热会生成铜和二氧化碳,所以A是氧化铜,E是一氧化碳,氧化铜会与溶液B反应,所以B是盐酸或硫酸,C是硫酸铜或氯化铜,C和氢氧化钠反应会生成蓝色沉淀D,所以D是氢氧化铜沉淀,然后将推出的物质进行验证即可.
解答 解:(1)A-K为中学常见的物质,H是一种建筑材料的主要成分,H是白色沉淀,所以H是碳酸钙,气体F和溶液G反应会生成碳酸钙,所以F是二氧化碳,G是氢氧化钙,固体I和硝酸银反应会生成蓝色溶液和银白色固体K,所以I是铜,J是硝酸铜,K是银,A为黑色粉末,A和气体E加热会生成铜和二氧化碳,所以A是氧化铜,E是一氧化碳,氧化铜会与溶液B反应,所以B是盐酸或硫酸,C是硫酸铜或氯化铜,C和氢氧化钠反应会生成蓝色沉淀D,所以D是氢氧化铜沉淀,经过验证,推导正确,所以D是Cu(OH)2,F是CO2;
(2)反应①是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,基本反应类型是复分解反应;
(3)反应②是硝酸银和铜反应生成硝酸铜和银,化学方程式是:Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)通过推导可知,E是一氧化碳,可以用来冶炼金属.
故答案为:(1)Cu(OH)2,F是CO2;
(2)复分解反应;
(3)Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)冶炼金属.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
11.根据下列实验方案进行实验,能达到相应实验目的是( )
| A. |  比较Zn和Fe的金属活动性强弱 | B. | 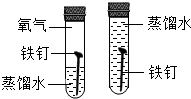 探究铁钉生锈时O2是否参与反应 | ||
| C. |  比较红磷和白磷的着火点 | D. |  测定空气中O2的含量 |
12.下列四个短语中,其原意一定包含化学变化的是( )
| A. | 花香四溢 | B. | 海市蜃楼 | C. | 木已成舟 | D. | 蜡炬成灰 |
9.下列措施有利于生态文明建设的是:( )
①研发易降解生物化肥 ②限制生产含磷的洗衣粉 ③田间焚烧秸秆 ④应用高效洁净的能源⑤加快化石燃料的开发与使用.
①研发易降解生物化肥 ②限制生产含磷的洗衣粉 ③田间焚烧秸秆 ④应用高效洁净的能源⑤加快化石燃料的开发与使用.
| A. | ①③⑤ | B. | ①②④ | C. | ②③⑤ | D. | ②④⑤ |
6.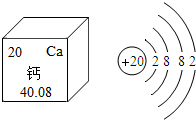 如图是钙元素在元素周期表中的信息及钙原子的原子结构示意图,下列关于钙元素的说法错误的是( )
如图是钙元素在元素周期表中的信息及钙原子的原子结构示意图,下列关于钙元素的说法错误的是( )
 如图是钙元素在元素周期表中的信息及钙原子的原子结构示意图,下列关于钙元素的说法错误的是( )
如图是钙元素在元素周期表中的信息及钙原子的原子结构示意图,下列关于钙元素的说法错误的是( )| A. | 核内有20个质子 | |
| B. | 相对原子质量是40.08 | |
| C. | 属于非金属元素 | |
| D. | 在化学反应中,钙原子易失去两个电子 |
13.下列选项正确的是( )
| A. | 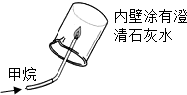 检验甲烷燃烧有CO2生成 | B. | 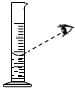 读液体体积 | ||
| C. |  将带有残留夜的滴管倒持 | D. |  吹灭酒精灯 |
10.氨基钠(NaNH2)是生产维生素A的原料.工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至一定温度生成氨基钠和氢气.下列说法不正确的是( )
| A. | NaNH2中氮元素的化合价为-3价 | |
| B. | NaNH2中钠元素的质量分数为35.9% | |
| C. | 钠的熔点比铁的熔点低 | |
| D. | 该反应的化学方程式为:4Na+4NH3$\frac{\underline{\;\;△\;\;}}{\;}$4NaNH2+H2↑ |
