题目内容
7. 化学就在我们身边,请用所学的化学知识填空.
化学就在我们身边,请用所学的化学知识填空.(1)现有H、C、N、O、Na五种元素,请选用其中的元素写出下列物质的化学式:
①人体中含量最多的物质H2O; ②实验室中常用的燃料C2H5OH;
③可以形成酸雨的气体NO2;④侯德榜是我国制“碱”先驱,这里的“碱”指Na2CO3.
(2)如图为某抗酸药的实物图,回答下列问题:
①图中属于有机合成材料的是塑料;该药物中淀粉属于B (填字母序号).
A.蛋白质 B.糖类 C.油脂 D.维生素
②图中塑料包装废弃后可用于微型实验.它的作用和优点都与我们实验室的点滴板(填一种仪器的名称)相近.
③图中铝箔常温下有优良抗腐蚀性,其原因4Al+3O2=2Al2O3.(用化学方程式表示)
④药片中的氢氧化铝在治疗胃酸过多患者时,发生的化学反应方程式:Al(OH)3+3HCl=AlCl3+3H2O.
分析 (1)首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
(2)根据有机合成材料必须具备三个条件:一是有机物,二是人工合成,三是高分子化合物、淀粉属于糖类、图中塑料包装废弃后可用于微型实验,其作用和优点都与我们实验室的井穴板相近以及氢氧化铝和盐酸反应生成氯化铝和水进行解答.
解答 解:(1)①人体中含量最多的物质水; ②实验室中常用的燃料是酒精;③可以形成酸雨的气体是二氧化硫;④侯德榜是我国制“碱”先驱,这里的“碱”指的是纯碱碳酸钠.
(2)①铝箔属于金属材料、塑料属于有机合成材料;淀粉属于糖类;
②图中塑料包装废弃后可用于微型实验,其作用和优点都与我们实验室的井穴板相近;
③铝箔常温下有优良抗腐蚀性,其原因是铝易和氧气反应生成一层致密的氧化物薄膜,防止铝进一步被氧化.
④氢氧化铝和盐酸反应生成氯化铝和水,化学反应方程式:Al(OH)3+3HCl═AlCl3+3H2O.
故答案为:(1)H2O、C2H5OH、NO2、Na2CO3;(2)①塑料、B;②点滴板;③4Al+3O2=2Al2O3;④Al(OH)3+3HCl=AlCl3+3H2O.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在;解题时应注意只能从给出的元素中选择来组成物质.

练习册系列答案
相关题目
17.为探究Zn和Cu的金属活动性强弱,提供的试剂有:Zn、Cu、H2SO4溶液、CuSO4溶液、ZnSO4溶液.下列说法正确的是( )
| A. | 最多只能设计两种实验方案 | |
| B. | 选用上述试剂中的两种就可实现实验目的 | |
| C. | ZnSO4溶液中加入Cu不能探究金属活动性强弱 | |
| D. | 方案中涉及的化学反应都是置换反应 |
2.下列有关实验现象的描述正确的是( )
| A. | 红磷在空气中燃烧产生大量白色烟雾 | |
| B. | 氢气在空气中燃烧发出明亮的蓝色火焰 | |
| C. | 细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| D. | 向硫酸铜溶液中滴加氢氧化钠溶液,有蓝色絮状沉淀生成,加热后可变成黑色 |
12.下列叙述与事实不符合的是( )
| A. | 酸雨的pH<5.6,酸雨是CO2等气体溶于雨水形成的 | |
| B. | 洗涤剂具有乳化作用能除去餐具上的油污 | |
| C. | 将铁钉放在硫酸铜溶液中,铁钉上有红色固体附着,液体的质量减少 | |
| D. | 发生火灾时可用湿毛巾捂住口鼻,低下身子沿墙壁跑出火灾区 |
19.小伟同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但他在空气中点燃镁条时,却发现在生成的白色固体中还夹着少量的淡黄色固体.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小伟查阅资料,查到了下列几种物质的颜色:
其他同学认为不必查阅氯化镁的颜色,理由是空气的成分中不含氯元素
【提出猜想】分析资料,小伟认为淡黄色固体可能是镁与空气中的氮气(或N2)反应生成的.
【实验探究】小伟设计实验证实了自已的猜想.
【实验结论】根据小伟的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式(任写一个即可)2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
【反思与评价】通过上述实验,你对燃烧的条件有什么新的认识?燃烧不一定要有氧气参加.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小伟查阅资料,查到了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
【提出猜想】分析资料,小伟认为淡黄色固体可能是镁与空气中的氮气(或N2)反应生成的.
【实验探究】小伟设计实验证实了自已的猜想.
【实验结论】根据小伟的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式(任写一个即可)2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
【反思与评价】通过上述实验,你对燃烧的条件有什么新的认识?燃烧不一定要有氧气参加.
16.某校化学兴趣小组选用H2SO4与下表中的四种溶液进行“复分解反应条件”的实验探究.
(1)以上实验中,不能够发生复分解反应的是②;(填写序号)
(2)实验结束后,将上述废液倒入同一烧杯中,观察到有白色沉淀,过滤,取少量无色滤液进行如下探究:

综合上述反应,以及相关实验现象推断,无色滤液中一定含有的溶质包括氯化钠、氢氧化钠、氯化钡;
(3)下列有关利用实验(2)中无色滤液的设想中,合理的是C.
A.鉴别MgCl2溶液和MgSO4溶液:取样,分别滴加少量无色滤液,观察现象
B.制取NaCl溶液,向无色滤液中加入适量的Na2CO3溶液,充分反应后过滤
C.处理实验室中含有H2SO4的废水:向含有H2SO4的废水中加入适量的无色滤液.
| 组合序号 | ① | ② | ③ | ④ |
| 组合物质 | 稀H2SO4 NaOH溶液 | 稀H2SO4 NaCl溶液 | 稀H2SO4 Na2CO3溶液 | 稀H2SO4 BaCl2溶液 |
(2)实验结束后,将上述废液倒入同一烧杯中,观察到有白色沉淀,过滤,取少量无色滤液进行如下探究:

综合上述反应,以及相关实验现象推断,无色滤液中一定含有的溶质包括氯化钠、氢氧化钠、氯化钡;
(3)下列有关利用实验(2)中无色滤液的设想中,合理的是C.
A.鉴别MgCl2溶液和MgSO4溶液:取样,分别滴加少量无色滤液,观察现象
B.制取NaCl溶液,向无色滤液中加入适量的Na2CO3溶液,充分反应后过滤
C.处理实验室中含有H2SO4的废水:向含有H2SO4的废水中加入适量的无色滤液.
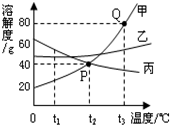 认真分析溶解度曲线图,回答下列问题.
认真分析溶解度曲线图,回答下列问题.