题目内容
1.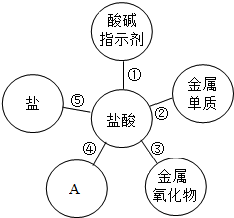 归纳是学习的重要方法,小红在复习盐酸的性质时归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习盐酸的性质时归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).(1)图中A所代表的物质类别是碱.
(2)为了验证性质③,可选用的物质是铁锈(填一种即可).
(3)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是ABD(填序号).
A.两种金属的大小 B.盐酸的质量分数
C.反应容器的大小 D.温度
(4)如用湿润的pH试纸测定盐酸的pH,则结果会偏大(填“偏大”、“偏小”或“无影响”).
分析 (1)根据盐酸能与酸碱指示剂、金属氧化物、活泼金属、盐、碱发生反应进行分析;
(2)根据铁锈的主要成分是氧化铁,氧化铁和盐酸反应会生成氯化铁和水进行分析;
(3)根据控制变量法就是创设相同的外部条件,并对所比较的量进行分析;
(4)根据盐酸在稀释后酸性减弱,pH值会偏大进行分析.
解答 解:(1)盐酸能与酸碱指示剂、金属氧化物、活泼金属、盐、碱发生反应,所以图中A所代表的物质类别是碱;
(2)铁锈的主要成分是氧化铁,氧化铁和盐酸反应会生成氯化铁和水,所以为了验证性质③,可选用的物质是铁锈;
(3)控制变量法就是创设相同的外部条件,因此探究镁和锌与盐酸反应的快慢,需要控制不变的条件就是对反应速度可能有影响的因素,分析知四个因素中只有容器的大小对反应速度无影响,故选:ABD;
(4)盐酸在稀释后酸性减弱,pH值会偏大.
故答案为:(1)碱;
(2)铁锈;
(3)ABD;
(4)偏大.
点评 熟练掌握酸的化学性质与酸碱盐之间的反应规律是解答本题的关键.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
2.把金属X放入硝酸铜溶液中,X表面有红色固体析出;若将Y放入硝酸铜溶液中,无明显现象.则X、Y、Cu三种金属活动性由强到弱的顺序是( )
| A. | X、Cu、Y | B. | Cu、X、Y | C. | X、Y、Cu | D. | Y、X、Cu |
3.一次用餐中,小丽对“固体酒精”产生好奇,于是她买回一袋,和同学一起对其进行研究.
【查阅资料】固体酒精中含有酒精、氢氧化钠等物质.
【提出问题】固体酒精中的氢氧化钠是否变质及变质的程度如何?
【提出猜想】小丽猜想:没有变质,只含有氢氧化钠.
小明猜想:全部变质,只含有碳酸钠.
你的猜想:部分变质,含有氢氧化钠和碳酸钠.
氢氧化钠在空气中变质的化学方程式CO2+2NaOH═Na2CO3+H2O.
【实验探究】小丽取少量固体酒精在水中充分溶解后过滤,取上述滤液于试管中,滴入几滴稀盐酸,无明显现象;小丽说氢氧化钠没有变质,小明认为她的结论不正确,其理由是氢氧化钠和碳酸钠同时存在时,加入少量盐酸,盐酸和氢氧化钠反应导致无明显现象,继续加入会有气泡,所以该结论不正确.
请你补全实验设计,填写表格中的①②③,证明固体酒精中氢氧化钠是否变质及变质的程度如何.
【拓展应用】除去部分变质的氢氧化钠溶液中的杂质,方法是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH或Ba(OH)2+Na2CO3=BaCO3↓+2NaOH(用化学方程式表示).
【查阅资料】固体酒精中含有酒精、氢氧化钠等物质.
【提出问题】固体酒精中的氢氧化钠是否变质及变质的程度如何?
【提出猜想】小丽猜想:没有变质,只含有氢氧化钠.
小明猜想:全部变质,只含有碳酸钠.
你的猜想:部分变质,含有氢氧化钠和碳酸钠.
氢氧化钠在空气中变质的化学方程式CO2+2NaOH═Na2CO3+H2O.
【实验探究】小丽取少量固体酒精在水中充分溶解后过滤,取上述滤液于试管中,滴入几滴稀盐酸,无明显现象;小丽说氢氧化钠没有变质,小明认为她的结论不正确,其理由是氢氧化钠和碳酸钠同时存在时,加入少量盐酸,盐酸和氢氧化钠反应导致无明显现象,继续加入会有气泡,所以该结论不正确.
请你补全实验设计,填写表格中的①②③,证明固体酒精中氢氧化钠是否变质及变质的程度如何.
| 实验操作 | 实验现象 | 实验结论 |
| ①用试管取少量滤液加入过量的稀盐酸,充分反应 (只能写足量或过量) | 有气泡产生 | 小丽猜想不成立 |
| ②用试管取少量滤液加入过量的氯化钙溶液,充分反应后,再加入 几滴酚酞溶液 | ③有白色沉淀产生,溶液变红色 | 你的猜想成立 |
20.下列有关化学符号“CO2”表示的意义,正确的是( )
| A. | 表示二氧化碳这种物质 | |
| B. | 二氧化碳由碳原子和氧原子构成 | |
| C. | 一个二氧化碳分子中含有一个氧分子 | |
| D. | 二氧化碳由一个碳元素和两个氧元素组成 |
6.与水相关的叙述正确的是( )
| A. | 电解水的化学方程式是H2O$\stackrel{通电}{→}$H2↑+O2↑ | |
| B. | 电解水产生的氧气和氢气的质量比为2:1 | |
| C. | 自来水生产中用氯气杀菌消毒 | |
| D. | 为防止水污染应禁止使用农药 |
11.下列除去物质中的少量杂质(括号内为杂质)的方法,正确的是( )
| A. | MnO2粉末(KCl)--溶解、过滤、洗涤、干燥 | |
| B. | CO(CO2)--通过足量的灼热氧化铜 | |
| C. | FeSO4溶液(CuSO4)--加入足量锌粉、过滤 | |
| D. | Na2SO4溶液(NaCl)--加入适量硝酸银溶液、过滤 |
 化学概念间有包含、并列、交叉等不同关系.下列选项符合如图所示关系的是( )
化学概念间有包含、并列、交叉等不同关系.下列选项符合如图所示关系的是( )