题目内容
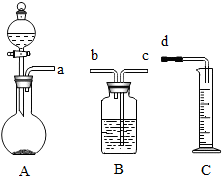 某兴趣小组用如图所示装置收集并测量反应产生的气体及其体积.若用该装置制取氢气,通过分液漏斗中加入30mL稀盐酸,与平底烧瓶中盛放的0.65g锌粒充分反应(盐酸足量).回答下列问题:
某兴趣小组用如图所示装置收集并测量反应产生的气体及其体积.若用该装置制取氢气,通过分液漏斗中加入30mL稀盐酸,与平底烧瓶中盛放的0.65g锌粒充分反应(盐酸足量).回答下列问题:(1)将右图装置连接成整套实验装置,连接顺序依次为:a→
(2)理论上0.65g锌与足量稀盐酸反应在该条件下应能收集到224mL的氢气,但3次实验收集到氢气体积的平均值约为242mL.造成误差的主要原因是
A.收集的气体包括了酸的体积 B.收集的气体包括了空气的体积.
(3)为了减小实验误差,制取氢气最好选用的酸是
考点:氢气的制取和检验,量气装置,气体的净化(除杂)
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)B装置中为便于水排出,应从b端进c端出;
(2)气体的质量增加,可能所用的盐酸浓度较大,有部分挥发的氯化氢气体;
(3)硫酸无挥发性,对实验结果无影响.
(2)气体的质量增加,可能所用的盐酸浓度较大,有部分挥发的氯化氢气体;
(3)硫酸无挥发性,对实验结果无影响.
解答:解:(1)要用图所示装置收集并测量反应产生的气体及其体积,B装置中为便于水排出,应从b端进c端出;故答案为:b、c;
(2)浓盐酸易挥发,所以测量值比理论值大,可能是使用的盐酸浓度较大,有部分挥发的氯化氢气体;故答案为:A;
(3)硫酸无挥发性,对实验结果无影响,所以最好选用稀硫酸制取氢气;故答案为:稀硫酸.
(2)浓盐酸易挥发,所以测量值比理论值大,可能是使用的盐酸浓度较大,有部分挥发的氯化氢气体;故答案为:A;
(3)硫酸无挥发性,对实验结果无影响,所以最好选用稀硫酸制取氢气;故答案为:稀硫酸.
点评:本题考查了实验室制取气体的装置选取,反应方程式及制取过程中的一些注意事项,能考查出学生对所学知识的应用和掌握情况.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质加入或通入紫色石蕊试液中试液会变色的是( )
| A、二氧化碳 | B、活性炭 |
| C、氯化钠 | D、氯化镁 |
下列物质投入水中,形成溶液的是( )
| A、泥沙 | B、面粉 | C、食盐 | D、色拉油 |
保护环境,保持空气清洁的有效措施( )
| A、植树造林 |
| B、禁止使用化肥农药 |
| C、减少城市人口 |
| D、加强工业废气排放的管理 |
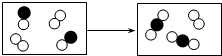 下列示意图形象地表示了A(
下列示意图形象地表示了A( )与B(
)与B(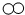 )反应生成C(
)反应生成C( )其反应前后分子及数目的变化,则该反应的化学方程式中,A、B、C的化学计量数之比为( )
)其反应前后分子及数目的变化,则该反应的化学方程式中,A、B、C的化学计量数之比为( )| A、1:1:1 |
| B、2:2:1 |
| C、2:1:2 |
| D、1:2:3 |
 2009年9月7日潍坊市政府与中国海洋石油总公司举行石油化工、盐化工一体化工程启动仪式.石油化工生产中,可通过反应制得甲烷、乙烯、丙烯、苯等重要有机物.请回答:
2009年9月7日潍坊市政府与中国海洋石油总公司举行石油化工、盐化工一体化工程启动仪式.石油化工生产中,可通过反应制得甲烷、乙烯、丙烯、苯等重要有机物.请回答: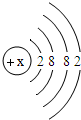 ,则该元素的原子序数为
,则该元素的原子序数为 水是一种重要的物质,在实验室和日常生活中有着十分重要的作用.请根据下列提示简要回答相关问题:
水是一种重要的物质,在实验室和日常生活中有着十分重要的作用.请根据下列提示简要回答相关问题: