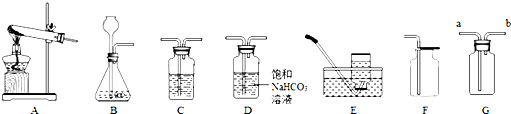
题目内容
2.某实验室用一氧化碳还原氧化铁制得铁,反应原理为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,若生成1.2g的铁,求参加反应的氧化铁的质量为多少?分析 根据氧化铁与足量一氧化碳充分反应的化学方程式和铁的质量,列出比例式,就可计算出参加反应的氧化铁的质量.
解答 解:设可得到铁的质量为x,
3CO+Fe2O3$\frac{\underline{\;点燃\;}}{\;}$2Fe+3CO2
160 112
x 1.2g
∴$\frac{160}{x}$=$\frac{112}{1.2g}$,
解之得:x=1.7g.
答:参加反应的氧化铁的质量为1.7g.
点评 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
10.某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中没有氢 元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.稀盐酸(稀HCl)
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
【交流与反思】由于过氧化钠常温下能与二氧化碳和水反应,所以保存一定要密封保存.
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中没有氢 元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.稀盐酸(稀HCl)
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量过氧化钠粉末于试管中,加入蒸馏水,再用带火星的木条伸入试管中 | 木条复燃 | 过氧化钠能与水反应生成氧气 |
| ②向上述反应后的试管中滴加酚酞试液 | 溶液变红 | 所得溶液呈碱性,推断过氧化钠与水反应生成NaOH NaOH(填化学式) |
13.为了对KCl 样品(含少量KNO3 )进行 分析,甲、乙、丙三位同学分别进行实验,他们实验数据如下表,请仔细观察和分析数据回答问题:(KCl+AgNO3═AgCl↓+KNO3)
(1)三位同学中乙同学所用KCl和AgNO3恰好完全反应(填编号)
(2)样品中KCl 的质量分数是多少?
(3)当KCl 和AgNO3 恰好完全反应后,将沉淀过滤,此时所得溶液中溶质的质量分数是多少?(结果保留到0.1%)
| 甲 | 乙 | 丙 | |
| 所取固体样品的质量/g | 20 | 10 | 10 |
| 加入AgNO3溶液的质量/g | 100 | 100 | 150 |
| 反应后所得沉淀的质量/g | 14.35 | 14.35 | 14.35 |
(2)样品中KCl 的质量分数是多少?
(3)当KCl 和AgNO3 恰好完全反应后,将沉淀过滤,此时所得溶液中溶质的质量分数是多少?(结果保留到0.1%)
10.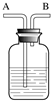 如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )
如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )
 如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )
如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )| A. | 导管B连接供给氧气的钢瓶 | |
| B. | 导管B连接病人吸氧气的塑胶管 | |
| C. | 该装置可用来观察输出氧气的速度 | |
| D. | 该装置可用来观察输出二氧化碳的速度 |
17.吸烟有害健康,香烟的烟气中含有几百种对人体有害的物质,尼古丁是其
中的一种,其化学式为C10H14N2,下列关于尼古丁的说法正确的是( )
中的一种,其化学式为C10H14N2,下列关于尼古丁的说法正确的是( )
| A. | 尼古丁中含有氮分子 | |
| B. | 尼古丁是由10个碳原子、14个氢原子、2个氮原子构成 | |
| C. | 尼古丁中氮元素质量分数最大 | |
| D. | 尼古丁由三种元素组成 |