题目内容
6.已知铜绿[Cu2(OH)2CO3]在加热时分解生成A、B、C三种常见的氧化物,下面是有关物质之间的转化关系图示.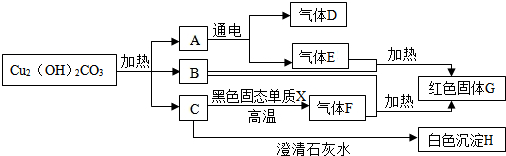
(1)试通过分析推断,写出下列物质的化学式:A,H2OFCO2.
(2)加热铜绿时发生反应的基本反应类型属于分解反应.
(3)写出C→H的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.
分析 根据图示分析解答,A在通电的条件下反应生成D和E,则A为水,D和E为氢气和氧气;B和E在加热条件下能生成红色固体G,则G为铜,所以B为氧化铜,那么E为氢气,D为氧气,碱式碳酸铜受热分解能生成氧化铜、水和二氧化碳;所以C为二氧化碳,C和黑色单质X反应生成气体F,并能够使石灰水变浑浊,所以X为碳单质,而H为碳酸钙,至此各物质鉴定完毕,可以据此答题.
解答 解:A在通电的条件下反应生成D和E,则A为水,D和E为氢气和氧气;B和E在加热条件下能生成红色固体G,则G为铜,所以B为氧化铜,那么E为氢气,D为氧气,碱式碳酸铜受热分解能生成氧化铜、水和二氧化碳;所以C为二氧化碳,C和黑色单质X反应生成气体F,并能够使石灰水变浑浊,所以X为碳单质,而H为碳酸钙,带入框图,推断合理;
(1)A是水,F是二氧化碳,故填:H2O;CO2;
(2)碱式碳酸铜受热分解能生成氧化铜、水和二氧化碳,属于分解反应,故填:分解;
(3)二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,故填:CO2+Ca(OH)2═CaCO3↓+H2O.
点评 此题主要是考查同学们的综合分析能力,要求同学们具备有关化合物的基础知识,并利用这些知识分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
相关题目
14.下列实验操作不正确的是( )
| A. | 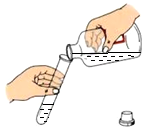 | B. | 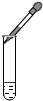 | C. |  | D. |  |
1.Cu(NO3)2溶液中加入一定量的铁粉,充分反应后,有金属析出,过滤、洗涤后往滤渣中加入稀盐酸,有无色气体放出,则滤液中一定存在的成份是( )
| A. | Cu(NO3)2 | B. | Cu(NO3)2和Fe(NO3)2 | C. | Fe(NO3)2 | D. | 无法确定 |
11.铺设钢轨时,为实现无缝焊接常用铝热剂反应2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3,此反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
18.下列说法中,正确的是( )
| A. | 煤炉上放一壶水可以防止CO中毒 | |
| B. | 生活中不能用煮沸方法降低水的硬度 | |
| C. | 金刚石、石墨都由碳原子直接构成,所以性质一样 | |
| D. | 氢气是最轻的气体 |
15.下列化学用于表示正确的是( )
| A. | 2个氯分子:2Cl2 | B. | 2个氢原子:H2 | C. | 铝的元素符号:AL | D. | 镁离子:Ma+2 |
16.下列各组的两种变化,都属于化学变化的一组是( )
| A. | 煤气燃烧、冰块融化 | B. | 茶杯破碎、剩饭变馊 | ||
| C. | 菜刀生锈、水果腐烂 | D. | 灯泡发光、人工降雨 |