题目内容
现有甲、乙、丙、丁四种元素,其中甲元素的一个原子核外只有一个电子;乙元素是地壳中含量最多的元素;丙元素的单质为黄色,它的一种氧化物是有刺激性气味的气体,属于空气污染物;丁元素的单质是空气中含量最多的气体.请回答下列问题:
(1)写出下列元素的名称:乙 ,丙 ;
(2)甲元素的单质是 (填化学式,下同),丁元素的单质是 ;
(3)丙元素的单质在乙元素的单质中燃烧的化学方程式是 ,反应的现象是 .
(1)写出下列元素的名称:乙
(2)甲元素的单质是
(3)丙元素的单质在乙元素的单质中燃烧的化学方程式是
考点:物质的鉴别、推断,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:元素推断题
分析:运用空气的成分、地壳中元素的分布与含量和原子的构成来解答该题.
根据原子中,核外电子数=质子数,“甲元素的原子核外只有一个电子”则甲元素为原子核内只有一个质子的氢元素;地壳中含量最高的元素应为氧元素;“丙元素的单质为黄色,它的一种氧化物是有刺激性气味的气体,属于空气污染物”,考虑为硫元素;空气中78%的为氮气,氮气是空气中含量最多的气体,据此分析解答即可.
根据原子中,核外电子数=质子数,“甲元素的原子核外只有一个电子”则甲元素为原子核内只有一个质子的氢元素;地壳中含量最高的元素应为氧元素;“丙元素的单质为黄色,它的一种氧化物是有刺激性气味的气体,属于空气污染物”,考虑为硫元素;空气中78%的为氮气,氮气是空气中含量最多的气体,据此分析解答即可.
解答:解:
①甲元素的原子核外只有一个电子,根据原子中,核外电子数=质子数,则甲元素为原子核内只有一个质子的氢元素;②地壳中含量最高的元素应为氧元素,则乙为氧元素;③“丙元素的单质为黄色,它的一种氧化物是有刺激性气味的气体,属于空气污染物”,则可推测丙为硫元素;④已知空气中78%的为氮气,而“丁元素的单质是空气中含量最多的气体”,所以丁元素为N元素;故:
(1)乙为氧元素,丙为硫元素;
(2)甲元素的单质是氢气,其化学式为 H2,丁元素的单质是氮气,其化学式为 N2;
(3)丙元素的单质在乙元素的单质中燃烧的化学方程式是 S+O2
SO2,反应的现象是产生淡蓝色火焰,放出大量的热,产生一种具有刺激性气味的气体.
故答案为:
(1)氧元素,硫元素;
(2)H2,N2;
(3)S+O2
SO2,产生淡蓝色火焰,放出大量的热,产生一种具有刺激性气味的气体.
①甲元素的原子核外只有一个电子,根据原子中,核外电子数=质子数,则甲元素为原子核内只有一个质子的氢元素;②地壳中含量最高的元素应为氧元素,则乙为氧元素;③“丙元素的单质为黄色,它的一种氧化物是有刺激性气味的气体,属于空气污染物”,则可推测丙为硫元素;④已知空气中78%的为氮气,而“丁元素的单质是空气中含量最多的气体”,所以丁元素为N元素;故:
(1)乙为氧元素,丙为硫元素;
(2)甲元素的单质是氢气,其化学式为 H2,丁元素的单质是氮气,其化学式为 N2;
(3)丙元素的单质在乙元素的单质中燃烧的化学方程式是 S+O2
| ||
故答案为:
(1)氧元素,硫元素;
(2)H2,N2;
(3)S+O2
| ||
点评:本题考查了空气的成分、地壳中元素的含量和原子的构成的相关知识,综合性强侧重基础注重学生综合运用知识的能力.

练习册系列答案
相关题目
下列不能用质量守恒定律解释的是( )
| A、3g镁在空气中燃烧得到氧化镁的质量大于3g |
| B、36g水通电完全分解得到4g氢气和32g氧气 |
| C、36g冰融化得到36g水 |
| D、3g高锰酸钾受热完全分解剩余固体的质量小于3g |
 (1)用化学符号表示:
(1)用化学符号表示:
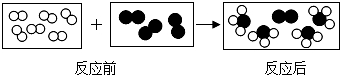
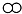 ”和“
”和“ ”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如下:
”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如下: