题目内容
为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小吴设计了一套实验装置(如图),他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量和质量分数)进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如下表:
| 反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
| 收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
| 乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 |
(1)由实验结果可知:金属活动性较强的是 .
(2)为了使得到的实验数据准确,小吴开始收集气体的时间点应该是 .
A.导管口一有气泡冒出时
B.冒出气泡连续且均匀时
C.检验产生的气体纯净时
(3)根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道 .
A.参加反应的硫酸质量
B.生成物中金属元素的化合价.

| 金属的化学性质. | |
| 专题: | 金属与金属材料. |
| 分析: | (1)根据相同时间内放出氢气的多少判断反应速率快慢,再利用反应速率判断金属活动性强弱; (2)根据实验的目的分析; (3)根据化学方程式计算金属的相对原子质量分析缺少的量. |
| 解答: | 解:根据表格数据可知相同时间内金属乙产生的气体比甲多,因此乙的活动性比甲强; (2)因为要测定金属产生氢气的快慢,因此应该是收集金属反应产生的所有气体,故是导管口一有气泡冒出时就要收集,故选项为:A; (3)已知金属的质量、产生氢气的质量,根据化学方程式进行计算金属的相对原子质量,因此缺少金属的化合价来书写化学方程式,故选项为:B; 故答案为:(1)乙;(2)A;(3)B. |
| 点评: | 本题属于金属活动性顺序的考查,熟练掌握金属活动性顺序的意义结合实验的目的分析得出结论即可,难度较大. |

下列净水方法中,净化程度最高的是( )
|
| A. | 静置 | B. | 过滤 | C. | 吸附 | D. | 蒸馏 |
建立模型是学习科学的重要方法,在理解化学反应的本质时往往引入模型,如图是某反应的微观模型,有关该模型的途述中,正确的是( )

|
| A. | 反应前后分子数目不变 | B. | 反应前后原子种类发生改变 |
|
| C. |
| D. |
|
 A.30℃时,甲溶液中溶质质量分数小于25%
A.30℃时,甲溶液中溶质质量分数小于25% 温能使乙物质的不饱和溶液变为饱和溶液
温能使乙物质的不饱和溶液变为饱和溶液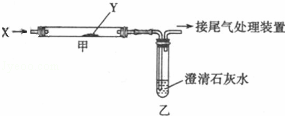
 和
和 化学性质相似
化学性质相似 是保持氧气化学性质的微粒
是保持氧气化学性质的微粒 一问题,小聪和同学们一起进行了如下的探究.
一问题,小聪和同学们一起进行了如下的探究.
 案的装置连接顺序(装置不重复使用),混合气体→ _________ →甲图装置(填装置编号).
案的装置连接顺序(装置不重复使用),混合气体→ _________ →甲图装置(填装置编号).