题目内容
9.回答下列问题:(1)实验室配制100g 10%的氯化钠溶液时,需要10g氯化钠固体.
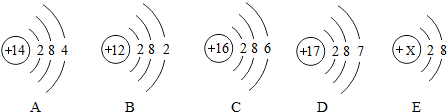
(2)称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g的砝码,则天平上的游码位置应是下图的B(填字母).

(3)下列仪器中,量取水时需要用到d和c仪器(填序号),溶解时需要用到e和a仪器(填序号).
a.烧杯 b.10mL量筒 c.100mL量筒 d.滴管 e.玻璃棒 f.药匙g.蒸发皿
(4)要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是D
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中
(5)用固体氢氧化钠配制50g20%的氢氧化钠溶液时,应该用①计算 ②称、量③溶解④转移贴标签等操作步骤.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)称量时如果用质量为23.1g的烧杯盛放固体,称量的氯化钠的质量为10g,即称量的总质量为33.1g,据此进行分析解答.
(3)从减小实验误差的角度去选择量筒的量程,量筒量程选择的依据有两点:一是保证测量一次,二是量程要与液体的取用量最接近;根据溶解操作所需的仪器,进行分析解答.
(4)配制溶液时,称取的溶质质量的多少或量取水的多少,都将直接影响溶液的配制结果;分析操作能否正确称量配制所需要的溶质和溶剂量,判断操作是否影响配制溶液的质量分数.
(5)用固体氢氧化钠配制50g 20%的氢氧化钠溶液,通常选用固体氢氧化钠溶解在一定水中而配制溶液的方法,需要溶质氢氧化钠的质量=50g×20%=10g,需溶剂水的质量=50g-10g=40g(合40mL).所设计的配制方案只要满足氢氧化钠10g、水40g即可完成配制.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,实验室配制100g10%的氯化钠溶液,需氯化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-10g=90g(合90mL).
(2)称量时如果用质量为23.1g的烧杯盛放固体,称量的氯化钠的质量为10g,即称量的总质量为33.1g,在托盘天平上已放30g的砝码,游码的质量应为3.1g,则天平上的游码位置应是图中的B.
(3)从减小实验误差的角度去选择量筒的量程,量筒量程选择的依据有两点:一是保证测量一次,二是量程要与液体的取用量最接近;量取90mL水时需要用到100mL量筒;先要向量筒中倾倒水,当接近刻度线时要改用胶头滴管滴加至刻度线,故要同时选择100mL量筒和胶头滴管.
溶解时需要用到烧杯和玻璃棒.
(4)A、游码没有回到零位就开始称量,使所称得食盐质量偏大,所配制的溶液质量分数偏高;
B、只在称量食盐的托盘垫上了干净的纸,忽略了纸的质量而使所称量的氯化钠质量偏低,配制的溶液质量分数偏小;
C、所用烧杯不干燥,有少量水,此时水的质量变大,所配制溶液的质量分数偏小;
D、溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中,此操作对溶质质量、溶剂质量已无影响,只是不符合操作规范.所以,对所配制溶液的质量分数没有影响.
故选D:
(5)选用固体氢氧化钠溶解在一定水中而配制溶液的方法,需要溶质氢氧化钠的质量=50g×20%=10g,需溶剂水的质量=50g-10g=40g(合40mL),然后称量出固体氢氧化钠,用量筒量取水40mL,溶解即可,所以用固体氢氧化钠配制50g 20%的氢氧化钠溶液的步骤包括:计算、天平称量、量筒量取、溶解.
故答案为:
(1)10;(2)B;(3)②c;a;(4)D;(5)溶解.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案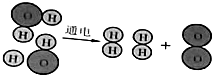 水通电分解的示意图,据图回答下列问题.
水通电分解的示意图,据图回答下列问题.| 反应物 | 生成物 | ||
| H2O | O2 | ||
| A | 18g | 2g | |
| B | 8g | 64g | |
| 质量比 | |||
(2)水通电分解过程中,原子的种类不变(填“改变”或“不变”,下同),各种原子的数目不变,而分子的种类改变.
(3)据图填写上表.
(4)由上表可知:任何一个化学反应都遵循质量守恒定律,不管反应物和生成物的质量是多少,各物质的质量比不变.
【实验目的】反应后溶液中的溶质有哪些?
【实验猜想】猜想一:Ca(OH)2、HCl 猜想二:CaCl2、HCl 猜想三:CaCl2、Ca(OH)2,猜想四:CaCl2.你认为猜想一不成立,原因是氢氧化钙和稀盐酸不能共存.
小组设计两种方案对猜想进行验证.
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取少量溶液,加入酚酞溶液 | 溶液不变色 | 猜想二成立 |
| 2 | 取少量溶液加碳酸钠溶液 | 产生气泡 | 猜想三不成立 |
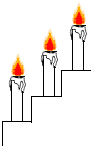 如图是三支高低不同的燃着的蜡烛,放在一只大的玻璃杯中,然后慢慢的往玻璃杯倒入二氧化碳气体,最先熄灭的是:下层的蜡烛,原因是二氧化碳的密度比空气大,而且不支持燃烧.
如图是三支高低不同的燃着的蜡烛,放在一只大的玻璃杯中,然后慢慢的往玻璃杯倒入二氧化碳气体,最先熄灭的是:下层的蜡烛,原因是二氧化碳的密度比空气大,而且不支持燃烧.