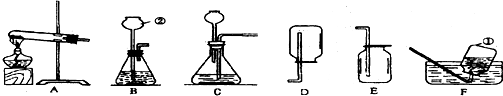
题目内容
19.某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”感到非常好奇,设计实验进行探究.【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【查阅资料】①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②CO2+2NaOH═Na2CO3+H2O.
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气.
(1)实验操作如图所示.
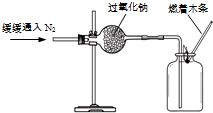
(2)实验现象及结论:观察到燃着木条熄灭现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气.
(1)同学们在老师的指导下设计了如图所示装置.其中A装置的作用是提供水蒸气,发生的变化是物理变化.
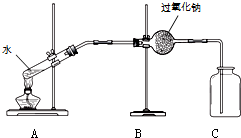
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
(1)同学们在老师的指导下设计了如图所示装置.
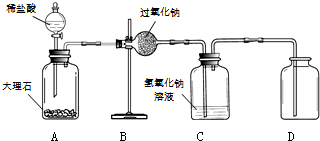
(2)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | 装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸. | A装置中观察到的现象有有气泡冒出,固体逐渐减少,C装置中有气泡出现. | A装置中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑; C装置作用是除去二氧化碳. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
(1)根据实验Ⅱ和Ⅲ,过氧化钠与二氧化碳或水蒸气反应后,还产生了另一种物质,该物质是化合物(填“单质”或“化合物”).
(2)某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气.
分析 【进行实验】实验Ⅰ:(2)如果过氧化钠与氮气发生反应生成氧气,则燃着的木头燃烧更旺;
实验Ⅱ:(1)根据题意判断;根据有无新物质是否生成判断物质的变化;
实验Ⅲ:(2)②大理石和稀盐酸反应生成二氧化碳气体判断反应现象;
【实验反思】(1)根据质量守恒定律判断元素的种类守恒;
(2)根据生成的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气进行解答;
解答 解:【进行实验】实验Ⅰ:(2)如果过氧化钠与氮气发生反应生成氧气,则燃着的木头燃烧更旺,如没反应,则燃着的木条熄灭,故填:燃着木条熄灭;
实验Ⅱ:(1)由题意知,A装置是把水加热至沸腾产生水蒸气,所以A装置的作用是提供水蒸气,液态的水变成水蒸气没生成新物质,是物理变化,故填:提供水蒸气;物理;
实验Ⅲ:(2)②大理石和稀盐酸反应生成氯化钙、水和二氧化碳,所以反应现象时有气泡产生,同时大理石逐渐减小;C装置作用是除去没反应掉的二氧化碳,能收集到较纯的氧气.故填:有气泡冒出,固体逐渐减少;CaCO3+2HCl=CaCl2+H2O+CO2↑;除去二氧化碳;
【实验反思】(1)根据质量守恒定律,反应物过氧化钠与二氧化碳或水蒸气反应后除了生成氧气,另一种物质中一定还含有钠、碳或氢元素,所以一定为化合物,故填:化合物
(2)因为生成的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气,故应先干燥二氧化碳,在和过氧化钠反应,故填:二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气.
点评 本题考查了过氧化钠与二氧化碳的反应及其反应产物氧气和碳酸钠的检验,完成此题,可以依据题干提供的信息以及已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.科学研究表明,氨气在常压下就可液化为液氮,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为:4NH3+3O2═2X+6H2O.下列说法中不正确的是( )
| A. | 氨气在常压下液化是物理变化,液氨具有可燃性属于化学性质 | |
| B. | 在生成X的过程中化学能转化成热能,X为空气中含量最多的气体 | |
| C. | 该反应为置换反应 | |
| D. | 液氨属于混合物 |
15.在常温下,下列各组物质能发生反应的是( )
| A. | 铁、硫酸铜溶液 | B. | 氢气、氧气 | C. | 碳、氧气 | D. | 镁、氧气 |
10.下列说法正确的是( )
| A. | 有盐和水生成的反应一定是中和反应 | |
| B. | 盐一定是由金属离子和酸根离子构成的 | |
| C. | 盐溶液不一定呈中性 | |
| D. | 根据酸、碱、盐的溶解性表,可判断酸、碱、盐的溶解度 |
7.小杰和小敬学习了碳单质的化学性质后,知道碳与氧气反应能够生成CO或CO2.于是两人联想到木炭粉与氧化铜发生的反应可能有:
①2CuO+C $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ ②CuO+C $\frac{\underline{\;高温\;}}{\;}$Cu+CO↑
他们想来自己的想法,请你同他们一起进行探究:
[猜想与假设]
木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;(2)产物是铜和二氧化碳;(3)产物是铜和一氧化碳、二氧化碳
[设计方案]
(1)检验产物中是否有CO2的方法是(用化学方程式表示)Ca(OH)2+CO2═CaCO3↓+H2O;
(2)如何检验产物中是否存在CO,两人查找了资料:CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝.CO有毒、有可燃性.
[实验与结论]
设计的实验装置(见图1)
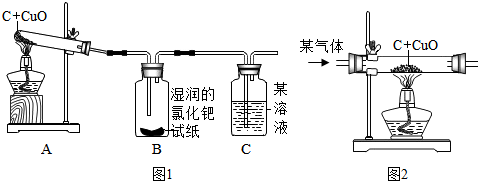
实验报告:
[反思与评价]
①实验结束时,为防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的胶塞取下,因此若没有B安全瓶,可能导致的后果是液体倒吸入试管把试管炸裂.
②根据实验结论,从环保角度考滤,上述装置C后应添加的装置是酒精灯,或塑料袋.
[拓展与交流]如果用图2装置代替图1中的A装置,这样既可以排尽试管中的空气,又能将反应的气体产物都“赶”出来,该气体可以是B (A.空气 B.氮气 C.氧气 )
①2CuO+C $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ ②CuO+C $\frac{\underline{\;高温\;}}{\;}$Cu+CO↑
他们想来自己的想法,请你同他们一起进行探究:
[猜想与假设]
木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;(2)产物是铜和二氧化碳;(3)产物是铜和一氧化碳、二氧化碳
[设计方案]
(1)检验产物中是否有CO2的方法是(用化学方程式表示)Ca(OH)2+CO2═CaCO3↓+H2O;
(2)如何检验产物中是否存在CO,两人查找了资料:CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝.CO有毒、有可燃性.
[实验与结论]
设计的实验装置(见图1)

实验报告:
| 实验现象 | 实验结论 |
| ①A中固体由黑色变红色 ②B中黄色试纸变蓝 ③C中澄清石灰水变浑浊 | ①有Cu生成 ②有CO生成 ③有CO2生成 |
①实验结束时,为防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的胶塞取下,因此若没有B安全瓶,可能导致的后果是液体倒吸入试管把试管炸裂.
②根据实验结论,从环保角度考滤,上述装置C后应添加的装置是酒精灯,或塑料袋.
[拓展与交流]如果用图2装置代替图1中的A装置,这样既可以排尽试管中的空气,又能将反应的气体产物都“赶”出来,该气体可以是B (A.空气 B.氮气 C.氧气 )