题目内容
11.写出下列物质的化学式:高锰酸钾KMnO4;硫酸钾K2SO4;氧化铁Fe2O3;氯化锌ZnCl2;氮气N2;氧化亚铁FeO;氢气H2;氢氧化铜Cu(OH)2;双氧水H2O2;二氧化锰MnO2;氩气Ar;四氧化三铁Fe3O4;氢氧化钙Ca(OH)2;硝酸铝Al(NO3)3;氯化镁MgCl2;碳酸氢铵NH4HCO3.
分析 根据物质的名称可以书写物质的化学式.
解答 解:高锰酸钾可以表示为KMnO4;硫酸钾可以表示为K2SO4;氧化铁可以表示为Fe2O3;氯化锌可以表示为ZnCl2;氮气可以表示为N2;氧化亚铁可以表示为FeO;氢气可以表示为H2;氢氧化铜可以表示为Cu(OH)2;双氧水可以表示为H2O2;二氧化锰可以表示为MnO2;氩气可以表示为Ar;四氧化三铁可以表示为Fe3O4;氢氧化钙可以表示为;Ca(OH)2硝酸铝可以表示为Al(NO3)3;氯化镁可以表示为MgCl2;碳酸氢铵可以表示为NH4HCO3.
故填:KMnO4;K2SO4;Fe2O3;ZnCl2;N2;FeO;H2;Cu(OH)2;H2O2;MnO2;Ar;Fe3O4;Ca(OH)2;Al(NO3)3;MgCl2;NH4HCO3.
点评 本题主要考查物质化学式的书写,比较简单,书写时要注意元素符号大小写问题.

练习册系列答案
相关题目
16.【提出问题】物质在发生化学反应前后,物质总质量是否会发生改变呢?
【猜想】①反应物总质量<生成物总质量.(填“>”或“<”或“=”)
②反应物总质量=生成物总质量.(填“>”或“<”或“=”)
③反应物总质量>生成物总质量.(填“>”或“<”或“=”)
【活动与探究】
【反思】①凡是化学(物理/化学)变化都符合质量守恒定律.
①方案一中天平不平衡的原因是:反应生成的二氧化碳气体逸出.
生活中有很多反应前后质量不变的现象,例如:纸燃烧我们发现前后质量轻了,原因是我们运用质量守恒定律时,我们关注反应物时忘了氧气,生成物时忘了水蒸气和二氧化碳;铁生锈时我们会发现质量前后重了,原因是我们运用质量守恒定律时,我们关注反应物时忘了水蒸气和氧气.所以,我们运用质量守恒定律时不能忘了反应物和生成物中的气体物质.
【猜想】①反应物总质量<生成物总质量.(填“>”或“<”或“=”)
②反应物总质量=生成物总质量.(填“>”或“<”或“=”)
③反应物总质量>生成物总质量.(填“>”或“<”或“=”)
【活动与探究】
| 实验方案 | 方案一 | 方案二 |
| 碳酸钠与盐酸反应的测定 | 铁钉与CuSO4溶液反应前后质量的测定 | |
| 天平是否平衡 | ||
| 实验现象 | 实验前:碳酸钠是 无色液体,盐酸是无色液体. 混合后瓶内产生气泡. | 混合前:硫酸铜溶液 蓝色,铁钉是黑色固体. 混合后:溶液呈浅绿色,铁钉表面有红色的物质. |
①方案一中天平不平衡的原因是:反应生成的二氧化碳气体逸出.
生活中有很多反应前后质量不变的现象,例如:纸燃烧我们发现前后质量轻了,原因是我们运用质量守恒定律时,我们关注反应物时忘了氧气,生成物时忘了水蒸气和二氧化碳;铁生锈时我们会发现质量前后重了,原因是我们运用质量守恒定律时,我们关注反应物时忘了水蒸气和氧气.所以,我们运用质量守恒定律时不能忘了反应物和生成物中的气体物质.
3.把一定质量的a、b、c、d四种物质散入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质量如下:
则:(1)表中“X”值为0.8;
(2)该反应的反应物是a和b,生成物是c;
(3)请写出这个反应的符号表达式a+b→c;
(4)该反应属于化合反应(填“化合”“分解”).
| 物质 | a | b | c | d |
| 反应前的质量(g) | 6.4 | 3.2 | 4.0 | 2.8 |
| 反应后的质量(g) | 5.2 | X | 7.2 | 2.8 |
(2)该反应的反应物是a和b,生成物是c;
(3)请写出这个反应的符号表达式a+b→c;
(4)该反应属于化合反应(填“化合”“分解”).
20.近年来,科学家在宇宙深处发现了H3和H3+粒子.下列有关说法中正确的是( )
| A. | 构成H3分子的原子的质子数为3 | B. | H3+和H3都可以表示一种单质 | ||
| C. | 一个H3+中含有3个质子、2个电子 | D. | 在1个H3和1个H3+中都含有3个中子 |
10.气体的溶解度与气体性质、溶剂有关,还与外界条件有关.“打开汽水瓶盖,汽水会自动喷出来”这种现象与下列外界条件存在主要关系的是( )
| A. | 压强 | B. | 温度 | C. | 汽水瓶 | D. | 光照 |
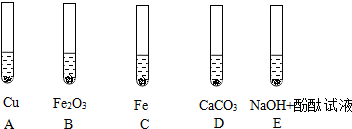
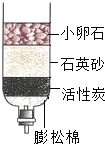 近年来云南省旱情严重,造成数万人饮水困难.水是生命之源,认识水资源、合理利用和保护水资源是我们义不容辞的责任.小冬同学制作的简易净水器如图所示:
近年来云南省旱情严重,造成数万人饮水困难.水是生命之源,认识水资源、合理利用和保护水资源是我们义不容辞的责任.小冬同学制作的简易净水器如图所示: