题目内容
19.2015年“世界水日”的主题是“水与可持续发展”.下列说法正确的是( )| A. | 液态水变成水蒸气时,水分子变大 | |
| B. | 过滤和加热均能使硬水转化为软水 | |
| C. | 蒸馏或用活性炭吸附均可使海水转化为淡水 | |
| D. | 电解水时负极和正极生成气体的质量比为1:8 |
分析 A、根据分子的基本性质解答:分子之间有间隔,在发生三态变化时,分子本身不变,只是分子间的间隔变化
B、根据硬水软化的方法分析;
C、根据活性炭具有吸附性分析;
D、电解水时负极和正极生成气体的质量比为1:8,体积之比是1:2;
解答 解:A、煮沸时液态水变成水蒸气,只是状态改变没有新物质生成,属于物理变化.在此变化过程中水分子之间的间隔增大了,而水分子本身的体积、质量、数目不变,故错误;
B、加热、蒸馏可使硬水软化,过滤时除去不溶性杂质,不能使硬水软化,故错误;
C、活性炭具有吸附性,能吸附色素和异味,但不能使海水淡化,故错误;
D、电解水时负极和正极生成气体的质量比为1:8,正确
故选:D.
点评 本题主要考查有关水的知识、分子的特点等,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.把A、B、C、D四种物质放在密闭容器内,在一定条件下反应,并测得反应物和生成物在反应前后的质量如下表所示:下列说法正确的是( )
| 物质 | A | B | C | D |
| 反应前质量/克 | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/克 | 待测 | 17.4 | 0 | 3.6 |
| A. | 该反应属于复分解反应 | |
| B. | 反应后密闭容器中A的质量是9.7克 | |
| C. | 物质C一定是化合物,物质D可能是单质 | |
| D. | 反应过程中,物质B和物质D变化的质量比为87:36 |
10.用H2和CuO反应的实验来测定水的组成,如图A所示.请回答下列问题:
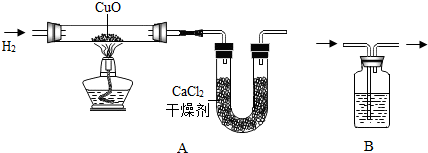
(1)试验中,用锌粒和稀硫酸反应制取氢气:检验氢气纯度后,先通一段时间氢气,再加热CuO进行反应.与CuO反应前,应将制取的H2通过图B所示装置,其中所盛的试剂是浓硫酸.
(2)试验中,测定的数据如表所示,根据数据计算生成的水中氢氧元素的质量比为:
(3)下列情况下,对试验测定结果一定没有影响的是①③(填序号)
①相对于CuO而言,H2是过量的 ②CuO粉末中含有不与H2反应的杂质 ③反应中部分CuO变成Cu2O ④干燥剂CaCl2有部分失效 ⑤用固体NaOH代替CaCl2做干燥剂.

(1)试验中,用锌粒和稀硫酸反应制取氢气:检验氢气纯度后,先通一段时间氢气,再加热CuO进行反应.与CuO反应前,应将制取的H2通过图B所示装置,其中所盛的试剂是浓硫酸.
(2)试验中,测定的数据如表所示,根据数据计算生成的水中氢氧元素的质量比为:
| 实验前 | 试验后 | |
| CuO和玻璃管总质量 | 65.6g | 59.2g |
| CaCl2和U形管的总质量 | 100.8g | 108.0g |
①相对于CuO而言,H2是过量的 ②CuO粉末中含有不与H2反应的杂质 ③反应中部分CuO变成Cu2O ④干燥剂CaCl2有部分失效 ⑤用固体NaOH代替CaCl2做干燥剂.
7.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 氢氧化钠 纯碱 NaOH | B. | 碳酸氢钠 小苏打 Na2CO3 | ||
| C. | 氢氧化钙 熟石灰 CaO | D. | 氯化钠 食盐 NaCl |
11.下列化学现象的描述,错误的是( )
| A. | 氢氧化钠固体溶于水放热 | |
| B. | 红磷在空气中燃烧发出白光,生成大量的白色烟雾 | |
| C. | 分别蘸有浓盐酸与浓氨水的玻璃棒靠近产生白烟 | |
| D. | 硫在氧气中燃烧发出明亮的蓝紫色火焰,放热,生成一种有刺激性气味的气体 |
8.下列各组物质在同一溶液中能大量共存的是( )
| A. | AgNO3、KNO3、HCl | B. | NaOH、CuSO4、HCl | ||
| C. | K2SO4、NaCl.Na2CO3 | D. | BaCl2、KNO3、NaCl |