题目内容
)(2014•邵阳)“嫦娥三号”于2013年12月2日,在西昌卫星发射中心发射,中国成为世界上第3个实现月球软着陆的国家.试回答:
(1)运载“嫦娥三号”的火箭外壳用到了钛合金,钛合金属于 (填“混合物”或“纯净物”).
(2)发射“嫦娥三号”的火箭所用燃料是偏二甲肼(C2H8N2),推进剂是四氧化二氮(N2O4),两者反应的化学方程式是:C2H8N2+2N2O4═3N2+2CO2+4X,则X的化学式是 .
(3)探月的目的之一是获取新能源﹣﹣氦.一个氦原子的原子核内有2个质子, 1个中子,则核外有 个电子.
1个中子,则核外有 个电子.
(4)月球富含钛铁矿,主要成分是钛酸亚铁(FeTiO3),其中钛(Ti)的化合价是 .

| 纯净物和混合物的判别;原子的有关数量计算;有关元素化合价的计算;质量守恒定律及其应用. | |
| 专题: | 化学式的计算;物质的微观构成与物质的宏观组成;化学用语和质量守恒定律;物质的分类. |
| 分析: | (1)根据合金的概念进行分析; (2)根据质量守恒定律的微观解释:化学反应前后,各原子的种类和数目不变; (3)根据原子中核内质子数=核外电子数分析; (4)根据在化合物中正负化合价代数和为零,进行解答. |
| 解答: | 解:(1)钛合金的主要成分是钛,属于混合物,故填:混合物; (2)根据质量守恒定律,化学反应前后,各原子的种类和数目不变.从化学方程式C2H8N2+2N2O4=2CO2+4X+3N2看,在化学反应前后(除X外),其它各原子个数差分别是:碳原子2﹣2=0,氢原子8﹣0=8,氮原子2+2×2﹣6=0,氧原子2×4﹣2×2=4,所以4X中共含有8个氢原子,4个氧原子.因此每个X中含有2个氢原子和1个氧原子,即X的化学式为H2O. 故填:H2O; (3)一个氦原子的原子核内有2个质子,根据原子中核内质子数=核外电子数可知,核外有2个电子,故填:2; (4)根据在化合物中正负化合价代数和为零,铁元素显+2,氧元素显﹣2,设钛元素的化合价是x,可知钛酸亚铁[FeTiO3]中钛元素的化合价:(+2)+x+(﹣2)×3=0,则x=+4.故填:+4. |
| 点评: | 本题难度不大,考查了物质分类的知识、质量守恒定律以及学生利用化合价 |

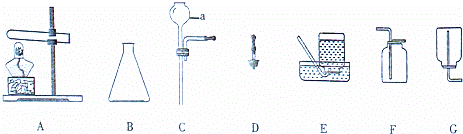
实验室配制50g溶质质量分数为6%的NaC1溶液的操作步骤有:计算、称量、量取、溶解.该实验过程中不需要用到的仪器是( )
|
| A. |
玻璃棒 | B. |
烧杯 | C. |
漏斗 | D. |
量筒 |
在电解水的实验中可以直接观察到的现象是( )

|
| A. | 水是由氢、氧元素组成 |
|
| B. | 有氢气和氧气产生,且体积比为2:1 |
|
| C. | 每个水分子是由两个氢原子和一个氧原子构成 |
|
| D. | 两电极均冒气泡,a管内气体与b管内气体的体积比约为2:1 |
下列粒子结构示意图表示不正确的是( )
|
| A. | 氢原子: | B. | 钠离子: | C. | 氯离子: | D. | 氧原子: |
在化学知识中有许多规律,下列具体物质的性质符合对应规律的是( )
|
| A. | 某些非金属氧化物能和碱反应生成盐和水;例如:二氧化碳和三氧化硫 |
|
| B. | 一般固体物质的溶解度随温度的升高而增大;例如:氢氧化钙和氯化钠 |
|
| C. | 常温下金属一般为固态;例如:汞和金 |
|
| D. | 某些非金属单质可以将金属从其氧化物中还原出来;例如:氢气和一氧化碳 |
 的原则计算指定元素的化合价的能力.
的原则计算指定元素的化合价的能力.
 入胶皮管内.
入胶皮管内.